Il calore sensibile o calore specifico sensibile è una grandezza fisica che è correlata alla variazione della temperatura di un corpo.
Esempio: Riscaldamento di una barra di metallo metal
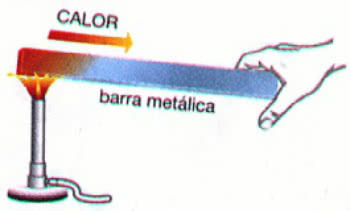
Nell'esempio sopra, il calore si propaga attraverso il conduzione termica. Questo processo comporta un aumento della temperatura del materiale, tuttavia, il suo stato fisico rimane lo stesso (solido).
Formula
Per calcolare il calore sensibile si usa la seguente formula:
Q = m. ç. Δθ
Q: quantità di calore sensibile (calce o J)
m: massa corporea (g o kg)
ç: calore specifico della sostanza (cal/g°C o J/Kg°C)
Δθ: variazione di temperatura (°C o K)
Nota: Per calcolare il calore sensibile dobbiamo conoscere il calore specifico che varia in ogni sostanza.
Leggi di più su: Calore specifico.
Calore sensibile e calore latente
Al Calore latente (L), lo stato fisico della sostanza si modifica, mentre in calore sensibile rimane lo stesso.
Un'altra differenza tra i due riguarda la temperatura. Cioè, il calore latente è indipendente dalla temperatura corporea, mentre il calore sensibile lo considera.
Un esempio di calore latente è lo scioglimento di un cubetto di ghiaccio o l'evaporazione dell'acqua. In entrambi i casi, la temperatura nei due stati fisici rimane la stessa.
Per calcolare il calore latente, utilizzare la seguente formula:
Q = m. l
Dove,
Q: quantità di calore (calce o J)
m: massa (g o kg)
l: calore latente (cal/g o J/Kg)
Leggi anche:
- Calore e temperatura
- calorimetria
- Bilancio termico
- Capacità termica
- Formule di fisica
Esercizi per l'esame di ammissione con feedback
1. (Mackenzie) Una fonte di calore fornisce calore continuamente, alla velocità di 150 cal/s, a una data massa d'acqua. Se la temperatura dell'acqua aumenta da 20°C a 60°C in 4 minuti, con il calore specifico dell'acqua di 1,0 cal/g °C, si può concludere che la massa dell'acqua riscaldata, in grammi, è:
a) 500
b) 600
c) 700
d) 800
e) 900
Alternativa e
2. (UFSM-RS) Si pone un corpo da 400 g e un calore specifico sensibile di 0,20 cal/g °C, ad una temperatura di 10 °C a contatto termico con un altro corpo da 200 g e calore specifico sensibile di 0,10 cal/g° C, alla temperatura di 60°C. La temperatura finale, una volta stabilito l'equilibrio termico tra i due corpi, sarà:
a) 14°C
b) 15°C
c) 20°C
d) 30°C
e) 40°C
Alternativa c
3. (UFPR) Durante l'eclissi, in una delle città della zona della totalità, Criciúma - SC, c'è stato un calo della temperatura di 8,0°C. (Ore Zero – 04/11/1994)
Sapendo che il calore specifico sensibile dell'acqua è 1,0 cal/g °C, la quantità di calore ceduta da 1000 g di acqua, quando si riduce la sua temperatura da 8,0 °C, nella calce, è:
a) 8.0
b) 125
c) 4000
d) 8000
e) 64000
Alternativa


