Kp è l'acronimo utilizzato per determinare il costante di equilibrio in termini di pressioni parziali. Questa costante funziona con i valori dei partecipanti gassosi di un equilibrio nell'unità atm, ad esempio.

Equazione che rappresenta una reazione chimica con componenti gassosi
In questa equazione, tutti i partecipanti sono gassosi, quindi quando un gas partecipante ha a pressione parziale nella miscela, è rappresentato dalla sigla pX.
Quando si imposta l'equazione di equilibrio chimico (in termini di concentrazione), i prodotti devono essere posti al numeratore e i reagenti al denominatore:
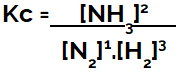
Kc espressione dell'equilibrio di formazione dell'ammoniaca
l'espressione di costante di equilibrio in termini di pressione (Kp) segue lo schema di Kc, cioè al denominatore si posizionano le pressioni parziali dei reagenti e al numeratore le pressioni parziali dei prodotti:
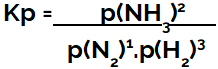
Kp espressione dell'equilibrio di formazione dell'ammoniaca
Osservazione: Se l'equazione di reazione di equilibrio chimico non presentare alcun partecipante gassoso, non si presenterà automaticamente Kp.
Esempio: (PUC-MG) Per la reazione: 2 CO(G) + O2(g)? 2 CO2(g), le pressioni parziali di CO(G) è il2(g) all'equilibrio sono rispettivamente 0.2 atm e 0.4 atm. La pressione totale del sistema è di 1,4 atm. Il valore di Kp per la reazione è:
a) 56.2
b) 40.0
c) 35,6
d) 28,4
e) 25,6
I dati forniti dall'esercizio sono:
pressione parziale di monossido di carbonio (pCO) = 0,2 atm;
Pressione parziale di monossido di carbonio (pO2) = 0,4 atm;
Pressione totale =1,4 atm;
Per determinare il Kp di questo sistema, dobbiamo eseguire i seguenti passaggi:
1° passo: Determinare la pressione parziale del monossido di carbonio (pCO2).
Per questo, ricorda solo che la pressione totale (pt) è la somma di tutte le pressioni parziali:
pt = pCO + pCO2 + PO2
1,4 = 0,2 + p (CO2) + 0,4
1,4 - 0,2 - 0,4 = pCO2
pCO2 = 0,8 atm
2° passo: Determinare il Kp dell'esercizio.
Per questo, basta usare i valori nell'espressione della costante di equilibrio Kp:
Kp = (pCO2)2
(pCO)2.(polvere2)1
Kp = (0,8)2
(0,2)2.(0,4)1
Kp = 0,64
0,04.0,4
Kp = 0,64
0,016
Kp = 40 atm-1
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-kp.htm
