Colloidi, soluzioni colloidali o sistema colloidale sono miscele che presentano l'aspetto di una soluzione, cioè una miscela omogenea. Ma in realtà sono miscele eterogenee.
Questo perché sebbene non sia chiara ad occhio nudo, la differenza nelle miscele colloidali può essere osservata attraverso l'uso di strumenti come il microscopio.
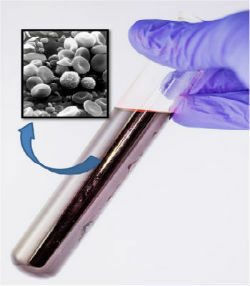
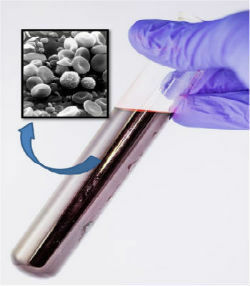 Il sangue, nonostante appaia omogeneo, con l'uso di un microscopio abbiamo osservato che è composto da più componenti.
Il sangue, nonostante appaia omogeneo, con l'uso di un microscopio abbiamo osservato che è composto da più componenti.
I colloidi sono presenti nella nostra vita quotidiana. Sono esempi di colloidi: crema idratante, yogurt, latte, sangue, coloranti e marmellata.
È per questo motivo che alcuni prodotti chimici indicano che devono essere agitati prima di essere utilizzati. Questo deve essere fatto per unire le particelle colloidali.
Allo stesso tempo, le miscele colloidali non si depositano naturalmente. Se mettiamo un colloide in un contenitore, le particelle non si depositano sul fondo. Inoltre non possono essere filtrati.
La dimensione delle particelle presenti nei colloidi è compresa tra 1 e 100 nanometri (1 nanometro equivale a 1 milionesimo di millimetro).
Tutto al di fuori di questa gamma sono miscele omogenee o eterogenee.
Le miscele omogenee sono considerate soluzioni vere. Le sue particelle sono più piccole di 1 nanometro. Le miscele eterogenee hanno particelle più grandi di 100 nanometri.
Impara di più riguardo Soluzioni chimiche e Separazione di miscele.
Quali sono le tue proprietà?
I componenti dei colloidi sono chiamati sparpagliato e disperdente. La quantità di disperdente è sempre maggiore.
Apparentemente, assumono una caratteristica di miscelazione omogenea.
Un esempio sono gli albumi montati sulla neve: il bianco in forma liquida assume il ruolo di componente disperso.
L'aria, che ha fatto sì che il bianco si trasformasse in schiuma, è il componente disperdente, poiché è necessaria più aria del bianco per ottenere questa miscela.
Inoltre, i colloidi consentono alla luce di passare tra di loro, il che non è il caso delle miscele omogenee.
Se puntiamo una torcia con un piccolo raggio di luce su una miscela colloidale, è possibile vedere un raggio di luce passare attraverso l'intero contenitore in cui si trova. È così che si chiama Effetto Tyndall.
Attraverso lo stesso esperimento, è anche possibile rilevare il movimento casuale delle particelle nella miscela. Questo è chiamato Movimento Browniano.
In breve, il proprietà dei sistemi colloidali sono:
- Le fasi della miscela non sono facilmente distinguibili;
- La gamma di dimensioni delle particelle è 1 e 100 nanometri;
- Effetto Tyndall;
- Presenza di particelle disperse e disperdenti;
- Non si depositano naturalmente, né possono essere filtrati;
- movimento browniano.
Tipi di colloidi
I colloidi sono classificati in base allo stato fisico delle particelle disperse e disperdenti.
I tipi di colloidi sono: aerosol, emulsione, schiuma, gel e sol (quelli che sembrano una soluzione). Scopri di più su ciascuno di essi:
Aerosol
Componente disperso: Solido o Liquido
Componente disperdente: gas
Esempi: Fumo, nebbia, nuvola, spray
Emulsione
Componente disperso: Liquido
Componente disperdente: Liquido o Solido
Esempi: Maionese, burro, formaggio, gelato
Schiuma
Componente disperso: gas
Componente disperdente: Liquido o Solido
Esempi: Panna montata, bianco nella neve, schiuma da barba, popcorn
Gel
Componente disperso: Liquido
Componente disperdente: solido
Esempi: Gelatina, gel di silice, dentifricio
Sole
Componente disperso: solido
Componente disperdente: Liquido o Solido
Esempi:Perla, Rubino, Sangue
Per saperne di più, scopri un metodo per separare le miscele colloidali, il Centrifugazione.