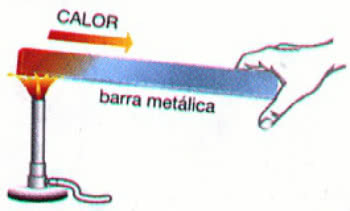
Equilibriotermico è la condizione in cui un corpo si trova nella stessotemperatura rispetto a ciò che li circonda. Si osserva che tutti i corpi che si trovano a temperature più alte dei loro vicini tendono a dar loro calore spontaneamente fino a quando entrambi iniziano a presentare la stessa temperatura.
Guardaanche:Fondamenti di Termologia
Equilibrio termico e legge zero della Termodinamica
L'equilibrio termico è il concetto centrale alla base della legge zero della termodinamica. Tale legge stabilisce che, nel caso in cui due sistemi termodinamici, IL e B, sono in equilibrio termico con un terzo sistema termodinamico, Ç, poi, IL e B saranno anche in equilibrio termico.
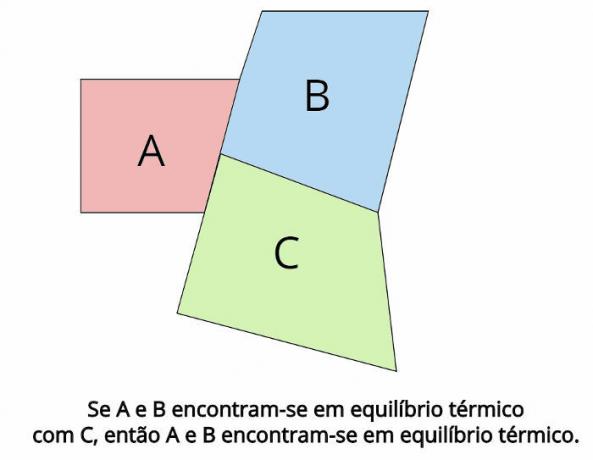
In equilibrio termico, le temperature finali di ciascun corpo devono essere uguali: TIL = TB = TÇ
Scopri cosa stabilisce l'enunciato della legge zero della Termodinamica:
“Se due corpi sono in equilibrio termico con un terzo corpo, allora quei corpi saranno in equilibrio termico tra loro”.
Un altro modo per comprendere l'equilibrio termico si basa sull'energia interna dei corpi. L'energia interna, o semplicemente energia termica, è una grandezza fisica
direttamenteproporzionale à temperatura del corpo. Pertanto, se ci sono corpi con temperature diverse all'interno dello stesso sistema termodinamico, avranno moduli diversi di energia interna e quindi trasferirà parte di quell'energia tra di loro fino a quando non ci sarà alcuna differenza tra le loro energie. interno. Vuoi saperne di più su cos'è l'energia interna e quali sono le sue proprietà? Accedi all'articolo: Energia interna.Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
calore ed equilibrio termico
Il trasferimento di calore avviene sempre spontaneamente, dal corpo con la temperatura più alta al corpo con la temperatura più bassa. Questo trasferimento di energia sotto forma di calore può avvenire attraverso processi quali guida, convezione e radiazione.
Guida: È il trasferimento di calore tra corpi che avviene soprattutto nei solidi. In questo tipo di conduzione non si verificano trasferimenti di massa. Questo tipo di trasferimento di calore spiega, ad esempio, come avviene l'equilibrio termico nei metalli.
Convezione: È un trasferimento di calore che avviene nei fluidi. In questa modalità di trasferimento del calore, vi è trasferimento di massa, poiché il fluido riscaldato si muove, formando correnti convettive fino a quando tutto il fluido raggiunge l'equilibrio termico.
Radiazione: È la trasmissione di calore attraverso onde elettromagnetiche, quindi questo processo avviene anche se non esiste un mezzo fisico tra il corpo e un altro corpo a temperature diverse. Il calore che viene trasferito, in questo caso, è l'equivalente di onde elettromagnetiche con energia inferiore a luce visibile, quindi radiazione termica, localizzata nella regione del infrarossi.
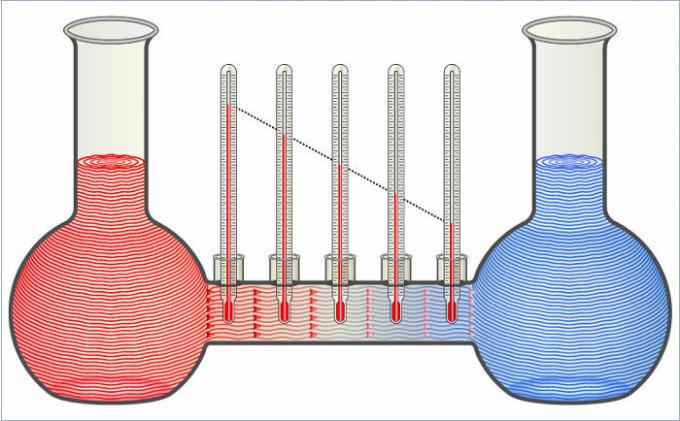
I due liquidi nella figura si trasferiscono calore l'uno all'altro fino a quando le loro temperature non sono uguali.
Vuoi saperne di più su come avviene ciascuno dei processi di trasferimento del calore? Accedi all'articolo: Processi di propagazione del calore.
calore sensibile
quando c'è differenzaneltemperatura tra due corpi, o tra un corpo e l'ambiente circostante, vi sarà uno scambio di calore tra loro spontaneamente, cosicché il il corpo a temperatura più alta si raffredda e i corpi a temperatura più bassa si riscaldano finché non raggiungono tutti la temperatura the nel equilibriotermico.
La quantità di calore che viene scambiata tra corpi a diverse temperature si chiama calore sensibile e questo importo può essere calcolato dalla formula mostrata nella figura seguente:
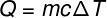
Q – calore (calce o J)
m – massa (g o kg)
ç - calore specifico (cal/gºC o J/kg. K)
T – variazione di temperatura (°C o K)
Nella formula sopra riportata, è importante sottolineare la grandezza del nome calore specifico. tale grandezza misura il quantità di energia per massa che una sostanza deve cedere, o assorbire, per far variare la sua temperatura di 1°C. Nel caso dell'acqua pura, ad esempio, e in condizioni di pressione normale, per variare la sua temperatura di 1°C, sono necessarie 1,0 calorie per grammo di acqua.
Pertanto, tutte le sostanze che hanno stabilito un contatto termico tra loro tendono a raggiungere la condizione di equilibriotermico nel tempo spontaneamente, tuttavia, alcuni richiedono una maggiore quantità di energia per farlo e questo influenza direttamente la temperatura per raggiungere l'equilibrio termico.
leggereanche:Che cos'è la temperatura?
Calore latente
È possibile che durante gli scambi di calore con l'ambiente circostante, un corpo presenti pressione, temperatura e volume che lo facciano subire un cambiamento nel suo stato fisico. Questi cambiamenti si verificano in temperaturacostante (per corpi composti da un'unica sostanza, senza impurità), cioè, pur ricevendo o cedendo calore all'ambiente esterno, la temperatura di questi corpi non cambia.
Questo è possibile solo perché tutta l'energia scambiata, in questo caso, viene utilizzata per modificare la conformazione delle tue molecole. Dal momento in cui la barriera energetica viene "superata" e tutto il contenuto del corpo si trova in un altro stato fisico, il Il corpo continua a scambiare calore con l'ambiente circostante, a meno che, naturalmente, la sua temperatura non sia uguale alla temperatura esterna.
oh Calore latente può essere calcolato dalla formula mostrata nella figura sottostante, controlla:
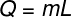
Q – calore latente (calce o J)
m – massa (g o kg)
l – calore specifico latente (cal/g o J/kg)
Formula di equilibrio termico
Nel caso volessimo scoprire qual è il temperaturanelequilibrio di qualche sistema termodinamico, è necessario considerare il sistema in questione come un sistemaisolato, cioè dobbiamo assumere che nessuna quantità di calore viene scambiata con le vicinanze di questo sistema.
Da questa condizione si può dire che l'intera quantità di calore scambiata viene scambiata solo tra i corpi che compongono questo sistema, tralasciando le dispersioni termiche per le pareti del contenitore, per esempio. In questo caso, diciamo che il contenitore ha capacità termica trascurabile, cioè non assorbe calore.
Immagina la seguente situazione: in una tazza di tè caldo, con una capacità termica trascurabile, versa dei cubetti di ghiaccio. Per determinare la temperatura di equilibrio termico, oltre a conoscere le condizioni iniziali del sistema, dobbiamo fare alcune considerazioni:
Tutta la quantità di calore che il tè caldo cede al ghiaccio sarà da esso completamente assorbito, poiché la tazza ha una capacità termica trascurabile.
Dobbiamo ignorare le perdite di calore nell'aria e in qualsiasi altro ambiente, in modo che questa tazza di tè possa essere intesa come un sistema termodinamico chiuso.
In questo modo possiamo stabilire che l'intera quantità di calore ricevuta dal ghiaccio è stata ceduta dal tè caldo, con questo abbiamo scritto la nostra formula per il calcolo del bilancio termico:
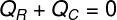
QR – Calore ricevuto
QÇ – calore ceduto
Il calore ceduto in (QÇ), si riferisce alla quantità di calore che il tè caldo ha ceduto ai cubetti di ghiaccio in esso inseriti. Già il calore ricevuto (QR) è la quantità di calore ricevuta da questi cubetti di ghiaccio. Questa quantità di calore avrà due nature: calore sensibile e caldo latente, poiché, per entrare in equilibrio termico, è probabile che i cubetti di ghiaccio si sciolgano.
Determinazione della temperatura di equilibrio termico
Determiniamo la temperatura di equilibrio termico dalla seguente situazione:
Una tazza, dalla capacità termica trascurabile, che contiene 200 ml (200 g) di tè ad una temperatura iniziale di 70°C, riceve 10 g di ghiaccio ad una temperatura di -10°C. Determinare la temperatura di equilibrio termico del sistema (assumere che il calore specifico del tè sia uguale al calore specifico dell'acqua):
Dati:
çACQUA = 1.0cal/g°C
çGHIACCIO = 0,5 cal/g°C
lGHIACCIO = 80 cal/g
Innanzitutto, consideriamo che tutto il calore ricevuto dal ghiaccio è stato ceduto dal tè:

Successivamente, è necessario dettagliare quali forme di calore sono state date e ricevute:
Tè: Il tè dava solo calore sensibile (QS), poiché le sue condizioni fisiche non sono cambiate.
Ghiaccio: Il ghiaccio inizialmente era a -10°C, quindi ha ricevuto calore sensibile (QS) fino alla temperatura di 0 ºC, quindi ha ricevuto calore latente (Ql) per liquefare. Dopo essere diventato liquido, ha ricevuto calore latente (QS) fino a raggiungere l'equilibrio termico (TF) con il tè.
Traducendo quanto analizzato sopra sotto forma di equazione, avremo il seguente calcolo da risolvere:
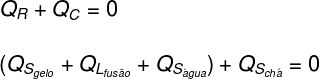
Sostituendo i dati forniti dall'esercizio nell'equazione trovata sopra, dovremo risolvere il seguente calcolo:
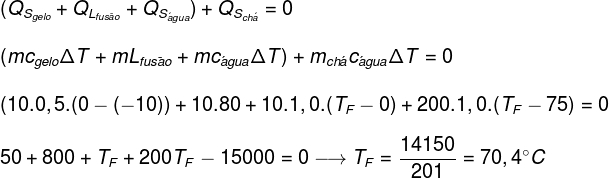
Secondo il calcolo fatto sopra, la temperatura di equilibrio del sistema tea+ice dovrebbe essere di circa 70,4°C.
Esperimento sull'equilibrio termico
Per testare l'equilibrio termico tra due corpi, possiamo eseguire diversi esperimenti. Il più semplice di questi, tuttavia, prevede l'uso di a calorimetro è un termometro. Il calorimetro è un contenitore adiabatico (che non permette il passaggio del calore), con capacità termica ditrascurabile, come una pentola rivestita di polistirolo, per esempio, che è un buon isolante termico.

Il calorimetro viene utilizzato per misurare la variazione di temperatura dell'impianto all'interno.
Bilancio termico e vita sulla Terra
oh equilibriotermico svolge un ruolo fondamentale nella vita terrestre. Senza la presenza di gas serra nell'atmosfera terrestre, la maggior parte dei radiazione termica del pianeta lo lascerebbe, propagandosi nello spazio. Nel tempo, ciò causerebbe un massiccio raffreddamento in tutto il pianeta, causando il congelamento degli oceani nel tempo.
Inoltre, gli oceani svolgono un ruolo chiave in equilibriotermico del pianeta. In virtù della sua grande pasta e calorespecifica, gli oceani sono dotati di un enorme capacitàtermico, cioè, hanno bisogno di ricevere enormi quantità di calore per cambiare la loro temperatura. Per questo motivo sono in grado di regolare la temperatura del pianeta in modo molto efficiente. Le regioni lontane dagli oceani e con poca acqua tendono ad avere grandi intervalli termici, come nel caso dei deserti, caldissimi di giorno e gelidi di notte.
quindi, il equilibriotermico è un processo di fondamentale importanza per il mantenimento dei processi fisici, chimici e biologici sul pianeta e, quindi, essenziale per l'esistenza della vita sulla Terra.
Di Me. Rafael Helerbrock