I legami covalenti possono verificarsi in forma molecolare o dativa e coordinata.
Legame covalente molecolare
In questo legame gli atomi si uniscono per la condivisione dei loro elettroni, quindi compaiono le coppie elettroniche indicate dal cerchio:
Legame covalente molecolare di due atomi di Cloro (Cl).
Ogni coppia elettronica formata contemporaneamente appartiene ai due atomi. Le molecole sono strutture elettricamente neutre perché non c'è né guadagno né perdita di elettroni, ma solo condivisione.
L'acqua è un composto molecolare formato da due atomi di idrogeno (H2) e un ossigeno (O).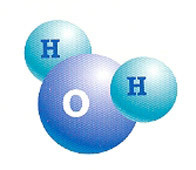
legame covalente dativo e coordinato
Questo legame obbedisce alla teoria dell'ottetto: gli atomi si uniscono cercando di acquisire otto elettroni nel guscio di valenza, cioè la configurazione elettronica dei gas nobili.
Quindi, un atomo che ha già raggiunto la stabilità elettronica si unisce a un altro che ha bisogno di elettroni per completare il guscio di valenza. Un esempio di questo legame è quando un atomo di zolfo si lega a due atomi di ossigeno per formare anidride solforosa (SO
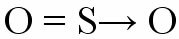
L'atomo di zolfo (S) acquisisce il suo ottetto con la formazione di un doppio legame con l'ossigeno situato a sinistra (legame coordinato), ma allo stesso tempo l'ossigeno posizionato a destra ha bisogno di elettroni per completare la sua ottetto. Appare quindi il legame covalente dativo rappresentato da un piccolo vettore (freccia). La freccia indica che il “S” sta donando una coppia di elettroni al “oh”.
Osserviamo la condivisione degli elettroni nella formazione del composto di anidride solforosa (SO3).
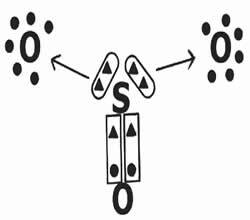
Si noti che l'elemento centrale (zolfo) stabilisce un doppio legame (coordinato) con uno degli ossigeni, ottenendo stabilità elettronica (otto elettroni nel guscio di valenza). Dona invece agli ossigeni due coppie di elettroni (legame dativo indicato dalla freccia →) nel tentativo di completare l'ottetto.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
di Liria Alves
Laureato in Chimica
Vedi altro!
Connessione in metallo
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
SOUZA, Liria Alves de. "Legame covalente "; Scuola Brasile. Disponibile in: https://brasilescola.uol.com.br/quimica/ligacao-covalente.htm. Consultato il 27 giugno 2021.

