Karena ada pengecualian pada aturan oktet, bagaimana kita mengetahui susunan yang benar antara atom dalam membentuk molekul?
Hal ini dapat dilakukan dengan menghitung beban formal masing-masing struktur. Muatan formal yang paling dekat dengan nol akan menjadi muatan dengan kemungkinan terbesar dari keberadaan aktual. Perhatikan bahwa ini "paling dekat dengan nol", jadi tidak harus nol.
Rumus muatan formal (Cuntuk) é:
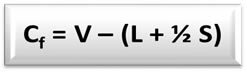
V = jumlah elektron valensi atom bebas;
L = jumlah elektron yang ada dalam pasangan atom yang terisolasi (non-ikatan) dalam struktur;
S = jumlah elektron yang dimiliki oleh atom dalam struktur.
Untuk memahami bagaimana ini terjadi, bayangkan kita ingin mengetahui struktur elektronik Lewis untuk molekul SO.2. Kami memiliki dua kemungkinan pengaturan antara atom:
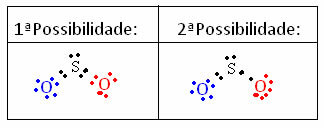
Muatan formal dari semua atom yang berpartisipasi dalam struktur dihitung. Lihat:
Kemungkinan 1:
Belerang (S): Oksigen (O) Oksigen (O)
Çf(S) = 6 – (2 + ½ 8) Çf(S) = 6 – (4 + ½ 4) Çf(S) = 6 – (4 + ½ 4)
Çf(S) =0 Çf(S) =0 Çf(S) =0
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
Kemungkinan ke-2:
Belerang (S): Oksigen (O) Oksigen (O)
Çf(S) = 6 – (2 + ½ 6) Çf(S) = 6 – (6 + ½ 2) Çf(S) = 6 – (4 + ½ 4)
Çf(S) = +1Çf(S) = -1 Çf(S) =0
Berdasarkan hasil yang diperoleh, kita dapat mencatat bahwa struktur pertama adalah struktur dengan probabilitas keberadaan nyata tertinggi. Jadi, kita tahu bahwa itu tidak mengikuti aturan oktet, tetapi belerang telah memperluas kulit valensinya, tetap stabil dengan 10 elektron.
Aturan ini juga berlaku untuk menemukan susunan ion yang benar.
Oleh Jennifer Fogaa
Lulus kimia
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
FOGAÇA, Jennifer Rocha Vargas. "Perhitungan Beban Formal"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/quimica/calculo-carga-formal.htm. Diakses pada 28 Juni 2021.


