Reaksi penetralan terjadi ketika asam bereaksi dengan basa membentuk air dan garam. Asam menyediakan ion H+ dan basa menyediakan ion OH- pembentukan air (H2HAI):
1 jam+(sini) + 1 OH-(sini) → H2HAI(ℓ)
Jenis reaksi ini disebut “netralisasi” karena pH medium dinetralkan; pH air adalah 7,0 (netral).
Agar reaksi ini terjadi, perlu untuk melepaskan sejumlah panas, karena hanya sebagian dari energi ion digunakan untuk membentuk ikatan yang menghasilkan molekul air, sedangkan sisa energi dilepaskan ke to cukup. Energi yang dilepaskan ini disebut Entalpi Netralisasi (∆Hpenetralan).

Karena melepaskan panas, itu sesuai dengan reaksi eksotermik, di mana entalpi (energi global sistem) akan selalu negatif, kurang dari nol.
Dalam kasus reaksi antara asam kuat dan basa kuat, nilai entalpi penetralnya akan selalu sama dengan – 13,8 kkal/mol atau – 57,7 kJ/mol. Hal ini terjadi karena basa dan asam kuat terdisosiasi sempurna dalam larutan dan, oleh karena itu, satu-satunya Reaksi yang bertanggung jawab untuk manifestasi panas adalah pembentukan air, seperti yang ditunjukkan pada tiga contoh di bawah ini:
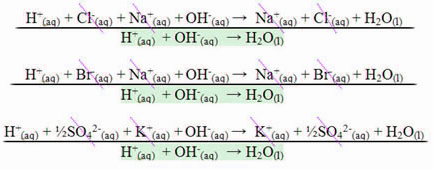
Dalam kasus reaksi penetralan yang melibatkan asam atau basa lemah, nilai entalpi penetralannya akan kurang dari –57,7 kJ/mol.
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/entalpia-neutralizacao.htm


