Az egyik legnagyobb kihívást annak, aki kémia-szakmát tanul, elektronikus disztribúciónak hívják. Amit ebben az összefüggésben bemutatunk, nagyban megkönnyítheti a Linus Pauling tudós által javasolt elektronkonfigurációval kapcsolatos tanulmányait.
Az egyes rétegekbe vagy energiaszintekbe illeszkedő elektronok maximális számát a táblázat adja meg:
Energiaszint réteg Az elektronok maximális száma
1. K 2
2. L 8
3. M 18
4. É 32
5 ° O 32
6. P 18
7. Q 8
Az alszintek növekvő energiarendje az átlósorrend sorrendje. A Linus Pauling-diagram az alábbiakban látható:
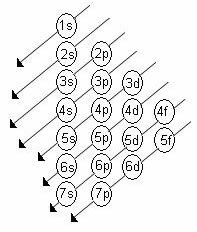
Alapszabályok:
1. Az elem atomszáma (Z) semleges állapotban az elosztandó elektronok számát jelzi. Ez a szám az elem szimbólumának bal alsó részén látható.
2. A Pauling-diagram segítségével kezdje el az elektronok eloszlását fentről lefelé, figyelembe véve az energia növekvő sorrendjét (a nyilak irányával orientálva).
3. Töltse ki az alszinteket az elektronok maximális szintjével. Ha egy adott alszint csak 6 elektronot tartalmaz, ne lépje túl ezt a mennyiséget.
4. Ellenőrizze az elektronok számát, összeadva azokat az egyes alszinteken.
Vigyük át a gyakorlatba?
Osszuk el a vasatom elektronjait (Z = 26).
Ha az atomszám 26, az azt jelenti, hogy a normál vasatomban 26 elektron van. A Pauling-diagram alkalmazásával:

Írta: Líria Alves
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/regras-distribuicao-eletronica.htm



