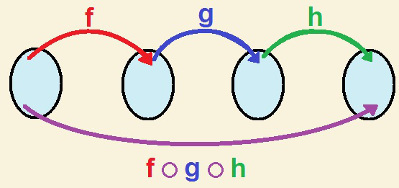
A sp típusú szénhibridizáció csak akkor történik meg, amikor két pi kötést (π) és két sigma kötést (σ) hoz létre. Ebben az esetben tehát két lehetőség van: a szén két kettős kötést vagy egyszeres és hármas kötést hozhat létre, az alábbiak szerint:
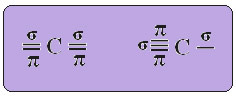
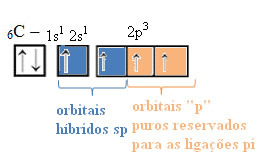
A szöveg "sp típusú hibridizáció3”Részletesen bemutatja, hogyan zajlik a szénhibridizáció. Emlékeztetve: a hibridizáció a tiszta atompályák „keverése”, amelyek hibrid atompályákból erednek, amelyek egyenértékűek egymással, de különböznek az eredeti tiszta pályáktól. Tehát ez az eredetileg így ábrázolt szénpályákon történik:
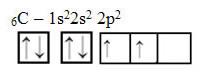
Az energia befogadásával azonban a 2s pályáról egy elektron (nyíllal ábrázolva) eljut a 2p pályára:
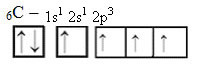
Így a szénnek négy párosítatlan pályája van, és négy, nem csak kettő, kovalens kötést képes létrehozni.
Sp típusú hibridizáció esetén tudjuk, hogy két kötés lesz pi; ezek a tiszta „p” pályákon fordulnak elő, míg a másik két pálya, amelyek sp hibridek, a fennmaradó szigma kötéseket hozzák létre.
Ennek az s és egy p pályának a hibridizációjának térbeli ábrázolása, amely hibrid sp orbitált eredményez, a következőképpen ábrázolható:
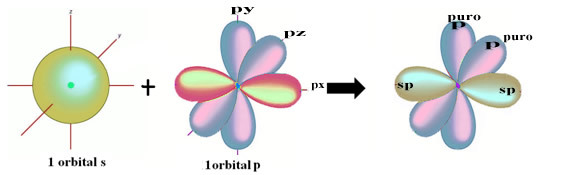
A fenti ábrán nagyon világos, hogy két tiszta pálya létezik, amelyek a pi kötéseket létrehozzák.
Ahhoz, hogy megértse, hogyan történik ez, vegyünk példaként egy cianidgáz (HCN) molekulát, amelyet az Egyesült Államokban használnak a gázkamrákban a halálbüntetésre ítélt foglyok számára. Szerkezeti képletét a következő adja:
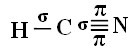
Ami a szént illeti, annak atompályái már bemutatásra kerültek, most nézzük meg a hidrogén és a nitrogén pályákat:
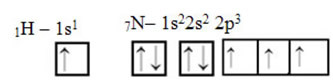
Vegye figyelembe, hogy az a párosítatlan hidrogénpálya, amely a szigma kötést végrehajtja, az „s”, amelyet térben egy kör jelöl és a nitrogénpályák „p” típusúak, amelyeket három kettős ovoid képvisel (mindegyik térben: x, y, z). Így a HCN molekula szerkezete a következőképpen jelenik meg:
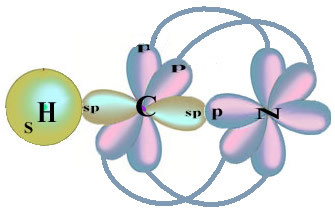
Ami az ebben a formaldehid szerkezetben létező kötések típusát illeti:
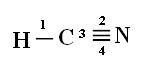
Kapcsolatok: 1 = σs-sp
2 = σp-sp
3 = 4 = πp-p
Írta: Jennifer Fogaça
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp.htm