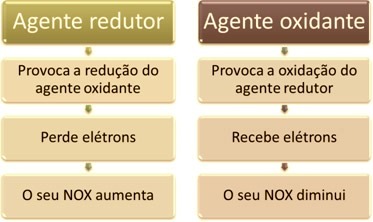
O NOX, vagy Oxidációs számpozitív vagy negatív töltésű szám, amely azt jelzi, hogy egy adott atom hiányos vagy nagyobb-e. elektronok száma, amikor kémiai kötést létesít egy másik atomtól, azzal azonos vagy attól eltérő, vagy a kémiai reakció. Így azt mondhatjuk, hogy:
pozitív NOX: azt jelzi, hogy az atom elektronhiányos;
negatív NOX: azt jelzi, hogy az atomnak nagyobb az elektronmennyisége.
Az atomok közötti kémiai kötés típusának ismeretében megtudhatjuk, hogy az atom NOX-e negatív vagy pozitív lesz-e. Néhány eset:
A) Az ionos kötelékben
Az ionos kötés mindig nem fém- vagy fém- és hidrogénatomokkal rendelkező fématomok között fordul elő. Mivel a fémek fő jellemzője az elektronok elvesztésére való hajlam, a hozzá kötött nemfém vagy hidrogén elektronokat fog kapni.
Így az alábbi esetekben:
1. eset: KI
A kálium fém, a jód pedig nem fém, ezért a kálium elveszíti az elektront, a jód pedig elektront nyer. Így arra a következtetésre jutunk, hogy:
Kálium: Pozitív NOX-értékkel rendelkezik.
Jód: Negatív NOX-értéke van.
2. eset: Nem
A nátrium fém, ezért elveszíti az elektront. A hidrogén viszont, amelyet nem minősítenek fémnek vagy nem fémnek, megkapja a nátrium által elveszített elektront. Így arra a következtetésre jutunk, hogy:
Nátrium: Pozitív NOX-értékkel rendelkezik
Hidrogén: Negatív NOX-értéke van
B) Kovalens kötés
Kovalens kötés történik:
Ametal és Ametal
Ametál hidrogénnel
hidrogén hidrogénnel
Mivel a kovalens kötés nem tartalmaz fémet, egyik érintett atom sem veszít el elektronokat. Mivel azonban az elektronegativitás (az elektronok vonzásának képessége egy másik atomtól) különbség van az atomok között, az egyik elektronja közelebb állhat a másikhoz.
Csökkenő sorrendje elektronegativitás atomok száma:
F> O> N> Cl> Br> I> S> C> P> H
Tehát:
1. eset: HCl
Mivel a klórnak nagyobb az elektronegativitása, mint a hidrogénnek, vonzza az elektronokat a hidrogén felé maga felé. Így azt mondhatjuk, hogy a klórnak több elektronja van, és a hidrogén elektronhiányos. Így arra a következtetésre jutunk, hogy:
Klór: Negatív NOX-értéke van
Hidrogén: Pozitív NOX-értékkel rendelkezik
2. eset: H2 ez a2
Mivel mindkét molekulában ugyanazok az atomok kölcsönhatásban vannak egymással, nem tudjuk felmérni az elektronegativitás különbségét. Ezért arra a következtetésre jutottunk, hogy mind a H2 mennyit az O-ban2, az egyes atomok NOX-értéke nulla.
Amellett, hogy meghatározzuk, hogy egy atomnak pozitív vagy negatív NOX-értéke van-e, meghatározhatjuk az elektronok számát is hogy elvesztette vagy megszerezte az ionos kötést vagy az elektronok mennyiségét, amelyhez a kötésben közeledett vagy eltávolodott kovalens. Ehhez a következő szabályokat alkalmazzuk:
1.) Egyszerű anyagok
atomjainak mindig lesz NOX nulla, mivel egyenlő atomok alkotják őket. Példák: Cl2 és tovább.
2.) Egyszerű ionos anyagok
Egy egyszerű ionos anyag atomjának NOX-ja mindig maga a töltés. Például:
1. példa: az ion Al+3 jellemzők NOX +3.
2. példa: az ion Cl-1 jellemzők NOX -1.
3.) Összetett anyagok
Az ionos vagy kovalens vegyületek azok, amelyek különböző kémiai elemeket tartalmaznak. A következőket kell figyelembe vennünk az egyes jelenlévő elemek NOX-értékének meghatározásához:
Ha van alkálifém (IA) vagy az elem Ezüst (Ag) a képlet bal szélén: ez mindig így lesz NOX +1.
ha van Alkáliföldfém (IIA) vagy az elem Cink (Zn) a képlet bal szélén: ennek mindig lesz NOX +2.
Ha van Boron család fémje (IIIA) a képlet bal szélén: ez mindig így lesz NOX +3.
Ha kalkogén van (VIA), a fémek kivételével ebben a családban, a képlet jobb szélén: ez mindig így lesz NOX -2.
ha van halogén (VIIA) a képlet jobb szélén: ez mindig így lesz NOX -1.
A vegyület képletében jelen levő bármely más kémiai elem NOX-értékét abból a tudatból határozzuk meg, hogy az összes atom NOX-értéke mindig 0 lesz.
Kövessük az összetett anyagok NOX-meghatározását egyes vegyületekben:
1. példa: PbI2.
A jódnak, amely halogén, NOX -1 van. Az ólom NOx-értékének (Pb) meghatározásához használja a következő kifejezést:
Pb NOX + I NOX (szorozva 2-vel) = 0
NOXPb + 2.(-1) = 0
NOXPb – 2 = 0
NOXPb = +2
2. példa: Au2s
A kén kalkogén, ezért NOX -2. A képletben a 2-es index mellett megjelenő Gold (Au) elem NOX-értékének meghatározásához használja a következő kifejezést:
Au NOX-értéke (szorozva 2-vel) + S NOx-értéke = 0
2. NOXAu + (-2) = 0
2. NOXAu – 2 = 0
2. NOXAu = +2
NOXAu = +2
2
NOXAu = +1
3. példa: Al2(CSAK4)3
Az oxigén (4.3-as indexével) kalkogén, ezért NOX -2. Az alumínium a bórcsaládba tartozik, és ezért NOX +3. A képletben az 1.3 index mellett megjelenő kén (S) elem NOx-értékének meghatározásához használja a következő kifejezést:
Al NOX-értéke (szorozva 2-vel) + (szorozva 2-vel) + O NOX-értéke (szorozva 12-vel) = 0
2. (+ 3) + 3. NOXs + 12.(-2) = 0
+6 + 3.NOXs – 24 = 0
3. NOXs = +24 – 6
3. NOXs = +18
NOXs = +18
3
NOXs = +6
4.) Vegyületion
Az összetett ion és egy vegyület közötti különbség az, hogy töltéssel rendelkezik a képlet összetételében. Lásd egy példát:
CSAK4-2
Az összes elem NOX-értékének meghatározására használt szabályok megegyeznek azokkal, amelyeket korábban az összetett anyagoknál alkalmaztunk. A különbség az, hogy az egyes jelenlévő atomok NOX összege mindig megegyezik a képletben szereplő töltéssel.
Kövessük a összetett ionokban lévő elemek NOX-értékének meghatározása:
1. példa: CSAK4-2
Az oxigén, amelynek indexe 4, kalkogén, ezért NOX -2. A kén (S) NOX-értékének meghatározásához használja a következő kifejezést:
S NOX + O NOX (megszorozva 4-vel) = -2 (vegyület ion töltése)
NOXs + 4.(-2) = -2
NOXs – 8 = -2
NOXs = -2 + 8
NOXs = + 6
2. példa: P2O7-4
Az oxigén, amelynek indexe 7, kalkogén, ezért NOX -2. A foszfor (P) NOX-értékének meghatározásához használja a következő kifejezést:
P NOX (szorozva 2-vel) + O NOX (szorozva 7-vel) = -4 (vegyület ion töltése)
2. NOXP + 7.(-2) = -4
2. NOXP – 14 = -4
2. NOXs = -4 + 14
NOXs = +10
2
NOXs = + 5
Általam. Diogo Lopes Dias
Forrás: Brazil iskola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-nox.htm