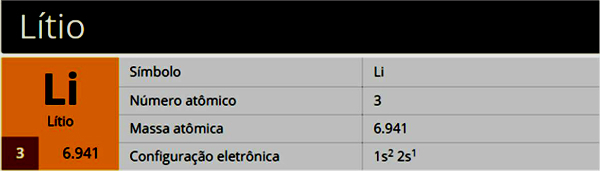
A lítium egy kémiai elem, amelynek Li szimbóluma, 3. atomszám, 7. atomtömeg, az 1. csoportba (1A család) tartozik, alkálifém.
Neve a görögből származik lithos, ami kőt jelent, mivel az elem kőzetekben található.
Jellemzők
Mivel nagyon reaktív elem, a természetben nem található el elszigetelten. Tiszta formájában levegő vagy víz jelenlétében könnyen oxidálódik.
A spodumene, a lepidolit és a petalite ásványi anyagokban található meg. A kőzetek mellett sós és termálvizekben is előfordul. Ipari környezetben lítium-klorid elektrolízissel nyerik.
Lágy, puha és ezüst színű fém jellemzi. A levegővel érintkezve szürke színt kap, ezért általában ásványi olajban tárolja.
Többek között a következők:
- Jó áramvezető;
- Rendkívül reaktív;
- Nagyon gyúlékony;
- Az alacsonyabb sűrűségű fém még kevésbé sűrű, mint a víz.
Tudjon meg többet, olvassa el még:
- Kémiai elemek
- Periódusos táblázat
alkalmazások
A lítiumnak különféle felhasználási módjai vannak, az ipari alkalmazásoktól a gyógyszergyártásig:
- Elemek gyártása lítiumionokból;
- Részt vesz a szívritmus-szabályozók működésében;
- A lítium-karbonátot pszichiátriai gyógyszerek készítésénél alkalmazzák, például bipoláris depresszió és nyugtatók ellen;
- Részt vesz a fémötvözetek kialakításában;
- Kenőanyagok gyártása magas hőmérsékleten működő gépekhez;
- Hőálló kerámia és üveg gyártása;
- Ipari szárító rendszerek lítium-klorid vagy bromid formájában.
Olvasson el más kémiai elemekről is:
- Bárium
- Foszfor
- Hélium


