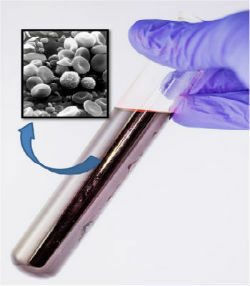
A diszperziók általában keverékekre vonatkoznak. Például, amikor sót keverünk vízzel, vagy sót és homokot, két diszperziót kapunk. Az anyagot, amely homogén (mint a só a vízben) vagy heterogén (mint a homok a vízben) terjed, „diszpergáltnak” nevezzük. A víz viszont diszpergálószerként működik ezekben az esetekben.
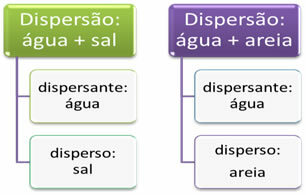
A két diszperzió közötti fő különbség a diszperzió részecskeméretében van. Míg a homokszemek szabad szemmel láthatók, a só részecskék láthatatlanok. Ennek alapján a diszperziók három fő típusba sorolhatók:
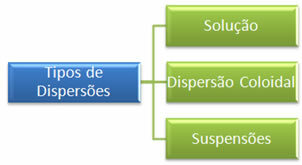
Vegye figyelembe, hogy az alábbi táblázatban a diszpergált részecskék méretének különbsége:

* Megoldások: homogén keverékek, amelyekben a szétszórt részecskéket mikroszkóp alatt sem láthatjuk. Néhány példa a fent említett vízzel kevert só, valamint a vízzel elkevert cukor.
Az oldatok esetében a diszperziót oldott anyagnak, a diszpergálószert oldószernek nevezzük. Az oldatokat semmilyen szűrési eljárással nem lehet elválasztani.
* Kolloid vagy kolloid diszperziók: néhány példa a majonéz és a zselatin. Részecskéit nem szabad szemmel vizualizálják, ezért gyakran összetévesztik őket homogén rendszerekkel, de valójában heterogének, amint az a mikroszkópok alkalmazásakor is megfigyelhető. Részecskéi nem a gravitáció hatására telepednek le, hanem csak ultracentrifugákkal.
Ne álljon meg most... A reklám után még több van;)
A kolloid diszperzióknak több típusa létezik: szol, szilárd szol, gél, emulzió, hab és aeroszol.
Az ilyen típusú diszperzió szétválasztása nem szűréssel lehetséges, hanem féligáteresztő membránnal. Részecskéi visszaverik és szétszórják a fényt.
* Felfüggesztések: heterogén rendszerek, amelyekben szabad szemmel még szemrevételezni is lehet részecskéiket. Néhány példa: homok a vízben, agyag a vízben, magnézium- és kalamintej.
Szétszóródások esetén a fény is visszaverődik. Elválasztása pedig közös szűréssel történhet.

* Bár néhány szerző és kutató azt javasolta, hogy a kolloid részecskék mérete 1 és 100 nm között legyen, a szuszpenziók pedig 100 nm-nél nagyobb, a kísérleti bizonyítékok hajlamosak ezt az értéket 1000 nm-re növelni, és ezt az értéket a legtöbben elfogadják szerzői. Makroszkopikus viselkedése azonban valóban meghatározza, hogy a keverék kolloid vagy szuszpenzió-e.
Írta: Jennifer Fogaça
Kémia szakon végzett
Hivatkozni szeretne erre a szövegre egy iskolai vagy tudományos munkában? Néz:
FOGAÇA, Jennifer Rocha Vargas. "A diszperziók típusai"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/quimica/tipos-dispersoes.htm. Hozzáférés: 2021. június 28.