A kolloidok, kolloid oldatok vagy kolloid rendszerek olyan keverékek, amelyek az oldat megjelenését mutatják, vagyis homogén keveréket. De valójában heterogén keverékek.
Bár szabad szemmel nem világos, a kolloid keverékekben a különbség olyan eszközök alkalmazásával figyelhető meg, mint a mikroszkóp.
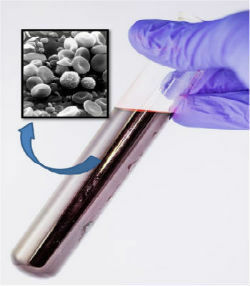 A vér, annak ellenére, hogy homogénnek tűnik, mikroszkóp segítségével azt tapasztaltuk, hogy több összetevőből áll.
A vér, annak ellenére, hogy homogénnek tűnik, mikroszkóp segítségével azt tapasztaltuk, hogy több összetevőből áll.
A kolloidok jelen vannak mindennapjainkban. Ők kolloidok példái: hidratáló krém, joghurt, tej, vér, színezékek és lekvár.
Éppen ezért egyes vegyi termékek jelzik, hogy használatuk előtt meg kell rázni őket. Ezt meg kell tenni a kolloid részecskék egyesítése érdekében.
Ugyanakkor a kolloid keverékek nem rendeződnek természetes úton. Ha egy kolloidot egy tartályba teszünk, a részecskék nem ülnek le az aljára. Szűrni sem lehet őket.
A kolloidokban jelenlévő részecskék mérete 1 és 100 nanométer között van (1 nanométer 1 milliméter milliméternek felel meg).
Minden ezen a tartományon kívül van homogén vagy heterogén keverékek.
A homogén keverékeket valós megoldásoknak tekintjük. Részecskéi kisebbek, mint 1 nanométer. A heterogén keverékek részecskéi nagyobbak, mint 100 nanométer.
Tudj meg többet Kémiai megoldások és Keverékek elválasztása.
Melyek a tulajdonságai?
A kolloidok összetevőit nevezzük elszórt és diszpergáló. A diszpergálószer mennyisége mindig nagyobb.
Nyilvánvalóan homogén keverési jellemzőt feltételeznek.
Az egyik példa a hófokra vert tojásfehérje: a folyékony fehér szín a diszpergált komponens szerepét tölti be.
A diszpergáló komponens a levegő, amelynek hatására a fehér habvá vált, mivel a keverék eléréséhez több levegő kellett, mint a fehér.
Ezenkívül a kolloidok lehetővé teszik a fény áthaladását közöttük, ez nem jellemző a homogén keverékekre.
Ha egy zseblámpát kis fénysugárral célzunk meg egy kolloid keverékre, akkor látható, hogy egy fénysugár áthalad az egész tartályon, ahol az található. Így hívják Tyndall-effektus.
Ugyanezen kísérlet segítségével a részecskék véletlenszerű mozgásának kimutatása is lehetséges a keverékben. Ezt úgy hívják Brown-mozgalom.
Röviden, a a kolloid rendszerek tulajdonságai ők:
- A keverék fázisai nem könnyen megkülönböztethetők;
- A részecskeméret-tartomány 1 és 100 nanométer;
- Tyndall-effektus;
- Diszpergált részecskék és diszpergálószerek jelenléte;
- Nem rendeződnek természetes úton, és nem is szűrhetők;
- Brown-mozgalom.
A kolloidok típusai
A kolloidokat a diszpergált és diszpergáló részecskék fizikai állapota szerint osztályozzák.
A kolloidok típusai: aeroszol, emulzió, hab, gél és szol (amelyek oldatnak tűnnek). Tudjon meg többet mindegyikről:
Aerosol
Szétszórt komponens: Szilárd vagy folyékony
Disperzáló komponens: gáz
Példák: Füst, köd, felhő, permet
Emulzió
Szétszórt komponens: Folyadék
Disperzáló komponens: Folyékony vagy szilárd
Példák: Majonéz, vaj, sajt, fagylalt
Hab
Szétszórt komponens: gáz
Disperzáló komponens: Folyékony vagy szilárd
Példák: Tejszínhab, hóban fehér, borotvahab, pattogatott kukorica
Gél
Szétszórt komponens: Folyadék
Disperzáló komponens: szilárd
Példák: Zselatin, szilikagél, fogkrém
Nap
Szétszórt komponens: szilárd
Disperzáló komponens: Folyékony vagy szilárd
Példák: Gyöngy, rubin, vér
Ha többet szeretne megtudni, ismerje meg a kolloid keverékek elválasztásának módszerét, a Centrifugálás.

