THE auto-oksi-redukcija ili nesrazmjerna reakcija je vrsta redoks reakcije u kojoj prolazi isti kemijski element oksidacija i smanjenje. Pogledajmo dva primjera ove vrste reakcija i kako ih uravnotežiti redoks metodom:
1. primjer:
NA2- + H+ → NE3- + NE + H2O
- Izračunavanjem oksidacijskih brojeva (NOX) svih atoma i iona koji sudjeluju u reakciji, moguće je provjeriti tko je oksidirao, a tko reagirao:
+3 -2 +1 +5 -2 +2 -2 +1 -2
NA2- + H+ → NE3- + NE + H2O
- Imajte na umu da je dušik vrsta koja je reagirala i oksidirala:
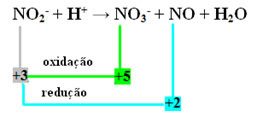
- Da bismo izvršili redoks balansiranje ove reakcije, NOX moramo povezati s proizvodima, a ne s reagensima:
NA3- = ∆Nox = 5 - 3 = 2
NO = ∆Nox = 3 - 2 = 1
- Invertirajući ∆NOX koeficijentima, imamo:
NA3- = ∆NOX = 2 → 2 bit će koeficijent NO
NO = ∆NOX = 1→ 1 bit će koeficijent NO3-
NA2- + H+ → 1 NA3- + 2 NE + H2O
- Ovime već znamo da u proizvodu ima 3 N, dakle koeficijent NO2- bit će 3:
3 NE2- + H+ → 1 NE3- + 2 NE + H2O
- Odrediti koeficijente H+ i od H2O, sjetite se da je broj primljenih elektrona jednak istoj količini doniranih elektrona; tako će naboj reagensa biti jednak naboju proizvoda. Na taj način možemo napraviti sljedeću shemu:
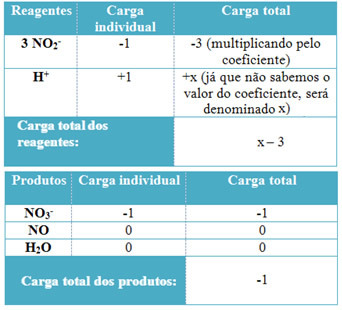
Na temelju tih podataka imamo da je ukupna napunjenost reagensa jednaka x - 3 a proizvod je jednak -1. Kao što je rečeno, optužbe njih dvojice moraju biti jednake. Kako već imamo ukupno opterećenje proizvoda, možemo izvršiti jednostavan izračun kako bismo znali kolika će biti vrijednost x:
x -3 = -1
x = -1 +3
x = 2
Dakle, koeficijent H+ je 2 i, prema tome, onaj H2Bit će 1:
3 NE2- + 2 H+ → 1 NE3- + 2 NO + 1 H2O
2. primjer:
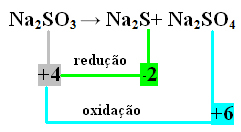
U ovom je slučaju S bio taj koji je istodobno prošao redukciju i oksidaciju. Dakle, kao što je prethodno učinjeno, NOX možemo povezati s proizvodima i obrnuti njihove vrijednosti, dodijelivši im koeficijente:
Na2 S = oxNox = 4 - (-2) = 6 → 6 bit će koeficijent Na2 SAMO4
Na2 SAMO4= OxNox = 6 - 4 = 2 → 2 bit će koeficijent Na2 s
Na2 SAMO3→ 2 Na2 Y + 6 Na2 SAMO4
Budući da u drugom kraku ima 8 sumpora, koeficijent Na2 SAMO3 bit će 8:
8 u2 SAMO3→ 2 u2 S + 6 u2 SAMO4
Napisala Jennifer Fogaça
Diplomirao kemiju
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/reacoes-auto-oxirreducao.htm
