intermolekularne sile to su načini na koje molekule spojeva (polarnih ili nepolarnih) nastalih kovalentnim vezama međusobno djeluju. Predložio ih je 1873. godine nizozemski kemičar i fizičar Diderik Van der Waals.
Prema Van der Waalsu, molekule mogu različito međusobno komunicirati. Te različite interakcije imaju velik utjecaj na talište (MP) i vrelište (PE) tvari. Dakle, intenzitet interakcije molekula definira njihov agregatno stanje (kruto, tekuće ili plinovito).
Uočiti postojanje različitih intermolekularnih sila (interakcija) jednostavno je, jer u prirodi možemo pronaći istu materiju u različitim fizičkim stanjima. Sada upoznajte tri vrste međumolekularnih sila koje mogu postojati između tvari nastalih kovalentnim vezama:
→ Londonske snage ili inducirane dipolom
To je vrsta sile koja se javlja između nepolarne molekule, to jest molekule koje nemaju polove (pozitivne i negativne), jer su elektroni ravnomjerno raspoređeni u njihovoj elektrosferi, kao na donjoj slici:
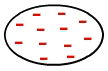
Ravnomjerna raspodjela elektrona u nepolarnoj molekuli
Međutim, u nekom se trenutku elektroni mogu akumulirati u području molekule, stvarajući u njoj negativni i pozitivni pol. Kako je ova molekula blizu druge, ovaj privremeni dipol na kraju inducira elektrone iz druge molekule da se skupe na jednom kraju, i tako dalje:

Stvaranje privremenog dipola u nepolarnoj molekuli
Dakle, molekule koje nisu bile polarne sada imaju inducirani dipol.
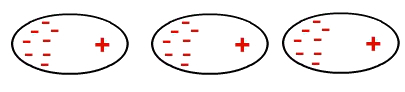
Dolazi do inducirane interakcije nepolarnih molekula
Neki primjeri supstancija čije molekule međusobno djeluju ovom vrstom sile su: ugljični dioksid (CO2), plin metan (CH4), plin etan (C2H6) i plinoviti vodik (H2).
→ Trajna dipolna ili dipolno-dipolna čvrstoća
To je vrsta intermolekularne sile koja se javlja između polarne molekule (osim onih koji imaju element vodik izravno vezan za fluor, kisik ili dušik). Neki primjeri tvari čije molekule međusobno djeluju dipol-dipol su klorovodična kiselina (HCl), sumporov dioksid (SO2), bromovodična kiselina (HBr) i cijanovodična kiselina (HCN).
Kako su molekule polarne (imaju pozitivne i negativne polove), one međusobno djeluju tako da se negativni pol jedne sjedini s pozitivnim polovom druge, i tako dalje:
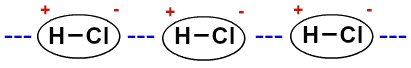
Prikaz trajnog dipola između molekula solne kiseline
Zbog prisutnosti dipola, budući da su molekule polarne, interakcija dipol-dipol intenzivnija je od induciranog dipola.
→ vodikove veze
To je vrsta intermolekularne sile koja se također javlja u polarne molekule, ali samo ako je atom vodika izravno povezan s jednim od tri kemijska elementa (fluor, kisik i dušik) plus elektronegativi periodnog sustava.
Neki primjeri molekula koje međusobno djeluju vodikovim vezama su: fluorovodonična kiselina (HF), amonijak (NH3) i vode (H2O).
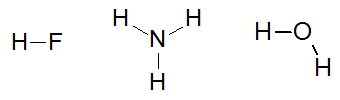
Strukturne formule tvari fluorovodična kiselina, amonijak i voda
Kako se vodikova veza javlja u molekulama čija je razlika u elektronegativnosti između atoma vrlo velika velika, to je intermolekularna sila visokog intenziteta (veća od dipol-dipola i dipola inducirani).
Pogledajte prikaz ove interakcije:
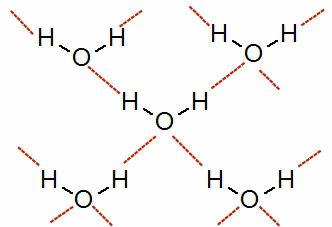
Prikaz vodikovih veza između molekula vode
Ja, Diogo Lopes Dias
Izvor: Brazil škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-forcas-intermoleculares.htm