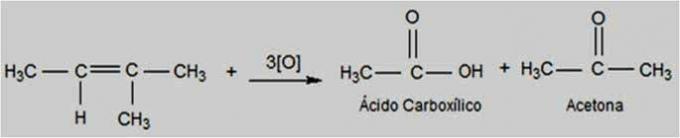
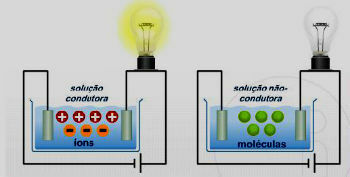
Na kovalentne veze, također nazvan molekularne ili homopolarne veze, jesu oni koji se javljaju između atoma elektronegativni elementi, to jest s tendencijom primanja elektrona uspostavljajući vezu dijeleći elektrone iz njihovih valentnih ljuski.
Kovalentna veza može se pojaviti između sljedećih elemenata: vodik, nemetali i polu metali. Metali nikada ne sudjeluju u ovoj vrsti vezivanja.
Razmotrimo jednostavan primjer kovalentne veze: veza koja stvara plinoviti vodik (H2):
H + H → H2
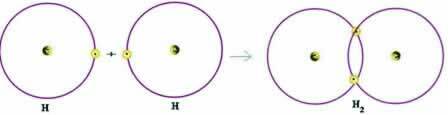
Imajte na umu da su oba atoma trebala primiti elektron kako bi dovršili svoju valentnu ljusku - prema Oktetskom pravilu - i, na taj način, ostali stabilni. Stoga su podijelili svoje elektrone i na taj su način oboje imali dva elektrona, imali su svoju kompletnu K-ljusku i stekli konfiguraciju plemenitog plina helija.
Ovo dijeljenje elektrona ono je što razlikuje ovu vrstu veze od ionske veze, u kojoj se odvija prijenos elektrona.
Pogledajte donju sliku za još dva primjera ovog slučaja:
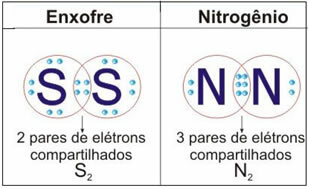
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
U ovoj vrsti veze dolazi do stvaranja molekula, koje mogu biti predstavljene njihovim odgovarajućim molekularne formule, odnosno najjednostavniji prikaz koji pokazuje koliko atoma svakog elementa ima u molekuli. Neki primjeri molekularnih formula su: H2, S2, O2, ne2, H2O, CO2itd.
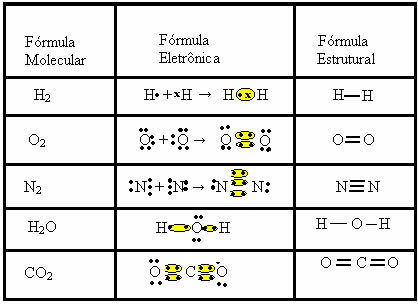
Kovalentnu vezu možemo predstaviti s dvije druge formule:
- Elektronička formula ili Lewisova formula: u ovoj formuli također se pojavljuju elektroni valentne ljuske svakog atoma i stvaranje elektroničkih parova. Te elektrone simboliziraju znakovi . ili x;
- Ravna strukturna formula ili Couper strukturna formula: prikazuje veze elemenata, pri čemu svaki zajednički par odgovara crtici. Ako je to samo crtica, nazivamo je jednom vezom; ako su dvije, dvostruka veza; a ako postoje tri crtice, trostruka veza.
Pogledajte druge primjere kovalentnih veza koje predstavljaju ove tri kemijske formule:
Napisala Jennifer Fogaça
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Kovalentne veze"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/ligacoes-covalentes.htm. Pristupljeno 27. lipnja 2021.