Čin otapanja skriva nekoliko misterija. Zašto se sve tvari ne pomiješaju u potpunosti s drugima?
Topljivost se može definirati kao sposobnost jedne tvari da se otopi u drugoj.
Opće pravilo topivosti glasi: "Slično se otapa slično". Ovo se pravilo odnosi na polaritet otapala i otopljene tvari i objašnjava činjenicu da se ulje ne otapa u vodi, ali je topljivo u benzinu.
Voda, poznata kao univerzalno otapalo, tvar je koja nastaje polarnim kovalentnim vezama u molekuli. Stoga voda otapa samo polarne otopljene tvari, poput soli, šećera, alkohola itd. Ulje se pak sastoji od nepolarnih veza i stoga se ne može miješati s vodom, već se miješa s benzinom jer je to također nepolarni spoj.
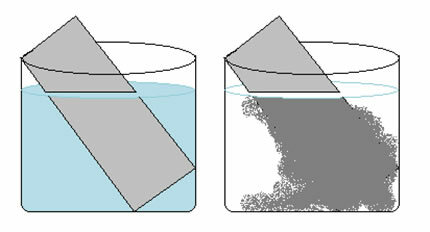
Sada razgovarajmo o količini otopljene tvari. Jeste li se ikad radoznali zapitali zašto kad miješamo čokoladu s hladnim mlijekom na dnu čaše uvijek ostane talog? To je ostatak proizvoda koji se nije otopio, ali zašto?
Postoji ograničenje količine otopljene tvari koja se može otopiti u određenoj količini otapala. Ali postoji i faktor koji otapanju može dati "mali potisak": temperatura otapala. Uzmite čašu mlijeka i stavite je na 1 minutu u mikrovalnu i promiješajte, što se događa? Svo čokoladno mlijeko otopit će se. Topivost krutina u tekućinama moguće je povećati s porastom temperature.
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Napisala Líria Alves
Diplomirao kemiju
Brazilski školski tim
Vidi više!
Riješenje - kvalitativni aspekti
Polarne i nepolarne organske molekule
Rješenja - Fizičko-kemijska
Kemija - Brazil škola
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
SOUZA, Líria Alves de. "Kako se tvari otapaju"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/como-as-substancias-se-dissolvem.htm. Pristupljeno 28. lipnja 2021.