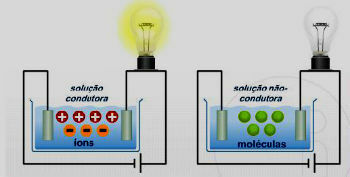
Proučavanje snage a kiselina je vrlo važan za određivanje sposobnosti kisele otopine da provodi električnu struju, jer se to odnosi na količinu iona koje ta tvar stvara u dodiru s vodom (ionizacija). Kad je kiselina prejaka, stvara previše kationova hidronija (H3O+) i mnogi anioni (X-). Pogledajte jednadžbu joniziranja bromovodične kiseline:
HBr + H2O → H3O+ + Br-
Pri ioniziranju vodik prisutan u molekuli kiseline stupa u interakciju s molekulom vode i stvara hidronij. Ali da bi se ovaj događaj dogodio, atom vodika mora nužno biti ioniziran. Ionizirajući vodik je onaj koji može stvoriti hidronijev kation.. Da bismo saznali je li vodik ionizirajući se, uzimamo u obzir klasifikaciju kiseline kao hidracidne (u svom sastavu nema kisika) ili oksidne kiseline (u svom sastavu ima kisika).
a) Hidracidi
Sav vodik u hidracidi smatra se ionizirajućim.
Primjeri:
- HCl: vodik koji se može ionizirati, stvarajući tako hidronij;
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
- H2S: Dva vodika koji se mogu ionizirati, a zatim se dobivaju dva hidrona
b) oksida kiselina
U oksidnoj kiselini, ionizira se samo vodik koji je u molekuli vezan za atom kisika. Za to je potrebno izgraditi njegovu strukturnu formulu. Pogledajte nekoliko primjera:
H3PRAH4 (fosforna kiselina)
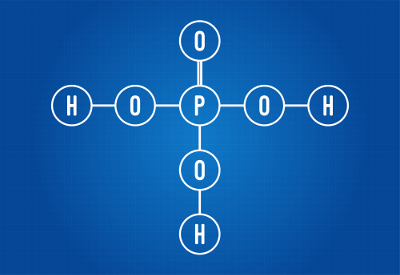
Strukturna formula fosforne kiseline
Vidimo da u strukturi fosforne kiseline postoje tri vodika vezana za kisik, pa postoje tri vodika koji se mogu ionizirati. Jednadžba ionizacije bit će:
H3PRAH4 + 3 H2O → 3 H3O+ + PO4-3
H2SAMO4 (sumporne kiseline)
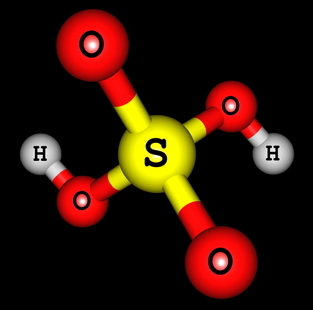
Strukturna formula sumporne kiseline
Možemo vidjeti da u strukturi sumporne kiseline postoje dva vodika vezana za kisik, pa postoje dva vodika koja se mogu ionizirati. Jednadžba ionizacije bit će:
H2SAMO4 + 2 H2O → 2 H3O+ + OS4-2
Ja, Diogo Lopes Dias
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
DANI, Diogo Lopes. "Ionizirajući vodikovi"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/hidrogenios-ionizaveis.htm. Pristupljeno 28. lipnja 2021.
Kemija

Disocijacija i jonizacija, talijanski znanstvenik Volta, električna struja, švedski fizikalni kemičar Svant August Arrhenius, teorija Arrhenius, pozitivni ioni, kationi, negativni ioni, anioni, kaustična soda, kuhinjska sol, polarne molekule, disocijacija ionski,