Prije uvođenja koncepta molarna masa i broj molova, pogledajmo neke važne definicije u ovom kontekstu:
→ Molarni pojam
Molar dolazi od riječi molekula, ali što je zapravo molekula? To je skup atoma koji su povezani kemijskim vezama.
→ Molekularna masa (MM)
Masu molekule moguće je izračunati zbrojem atomskih masa svakog atoma koji čine odgovarajuću molekulu. Rezultat se naziva Molekularna masa (MM).
Kolika bi bila molekulska masa sumporovodika (H2S) na primjer?
Prvo morate znati što atomska masa svakog atoma, što je dato Periodnim sustavom elementi.
Atomska masa vodika (H) = 1 a.m.u. (jedinica po atomskoj masi)
Atomska masa sumpora (S) = 32,1 a.u.u.
Molekularna masa je zbroj atomskih masa atoma.
Napomena: vodik molekule H2S ima koeficijent 2, pa njegovu masu morate pomnožiti s 2. Izračunavanje:
Molekularna masa H2S = 1 • 2 + 32,1 = 34,1 u
(H) + (S) = (H)2S)
Molarna masa i broj madeža
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Molarna masa, kao i broj madeža, povezani su s Avogadrova konstanta (6,02 x 1023) kroz sljedeći koncept:
'' Broj elementarnih entiteta sadržanih u 1 molu odgovara Avogadrovoj konstanti, čija je vrijednost 6,02 x 1023 mol-1.''
Stoga je molarna masa masa 6,02 x 1023 kemijskih entiteta i izražava se u g / mol.
Karta uma - Mol
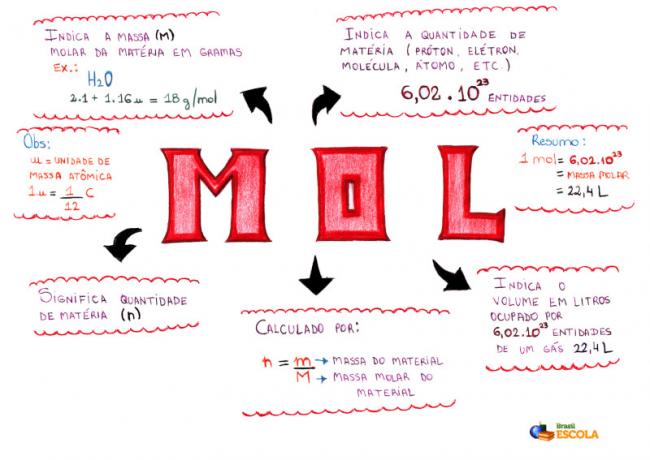
* Da biste preuzeli umnu mapu, Kliknite ovdje!
Primjer: H2s
Molekularna masa = 34,1 u
Molarna masa (M) = 34,1 g / mol
To znači da s 34,1 g / mol sumporovodika imamo 6,02 x 1023 molekule ili 1 mol molekula sumporovodika.
Zaključak
Molekularna masa i molarna masa imaju iste vrijednosti, ono što se razlikuje je mjerna jedinica. Molarna masa je povezana s brojem molova koji je dan Avogadrovom konstantom.
* Moja misaona karta, Diogo Lopes
Napisala Líria Alves
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
SOUZA, Líria Alves de. "Molarna masa i molski broj"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/massa-molar-numero-mol.htm. Pristupljeno 27. lipnja 2021.