O izračunavanje broja atomskih čestica koristi se za označavanje količine protona (u jezgri), elektrona (u elektrosferi) i neutrona (u jezgri) prisutnih u bilo kojem atomu ili ionu. Da biste to učinili, bitno je znati neke karakteristike atoma:
1- Atomski broj (Z)
Riječ je o matematičkom kodu predstavljenom velikim slovom Z, smještenom na donjoj lijevoj strani kratice atoma:
Zx
Označava broj protona (p) u jezgri i broj elektrona (e) u elektrosferi atoma. Dakle, općenito:
Z = p = e
2- Masni broj (A)
Riječ je o matematičkom kodu koji odgovara zbroju broja protona (p) i neutrona (n), oba prisutna u jezgri bilo kojeg atoma. Jednadžba koja predstavlja maseni broj dana je:
A = p + n
Budući da je broj protona jednak atomskom broju, možemo napisati jednadžbu za izračunavanje masenog broja na sljedeći način:
A = Z + n
Ako znamo maseni broj i atomski broj atoma, možemo odrediti broj neutrona na sljedeći način:
n = A - Z
3- ioni
Oni su atomi koji gube ili dobivaju elektrone. Imaju pozitivan ili negativan predznak pozicioniran u gornjem desnom dijelu njihovog prikaza, kao u sljedećem modelu:
x+ ili X-
Pozitivni ion: To se naziva kationom, a pozitivni znak pokazuje da je izgubio elektrone.
Negativni ion: To se naziva anionom, a negativni znak ukazuje da je dobio elektrone.
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
4- Atomske sličnosti
a) Izotopi
Atomi koji imaju jednak atomski broj i različite masene brojeve. Primjer:
7x14 i 7Y16
Atomi X i Y imaju jednak atomski broj (lijevo od kratice), odnosno jednak 7. Atom X ima maseni broj (s desne strane kratice) jednak 14, a atom Y ima maseni broj jednak 16.
b) izobare
Atomi koji imaju isti maseni broj i različite atomske brojeve. Primjer:
15x31 i 13Y31
Atomi X i Y imaju maseni broj (s desne strane kratice) jednak 31. Atom X, s druge strane, ima atomski broj jednak 15, a atom Y atomski broj jednak 13.
c) Izotoni
Atomi koji imaju različite masene brojeve i atomske brojeve, ali isti broj neutrona.
d) Izoelektronika
Atomi koji imaju jednak broj elektrona. Primjer:
12x+2 i 7Y-3
Atom X ima atomski broj jednak 12 i kation je (s pozitivnim nabojem +2), tako da gubi dva elektrona, tako da u svojoj elektrosferi ima 10 elektrona. Atom Y, s druge strane, ima atomski broj jednak 7 i anion je (s negativnim nabojem -3), pa dobiva tri elektrona, tako da u svojoj elektrosferi ima 10 elektrona.
Karta uma: Atomske čestice
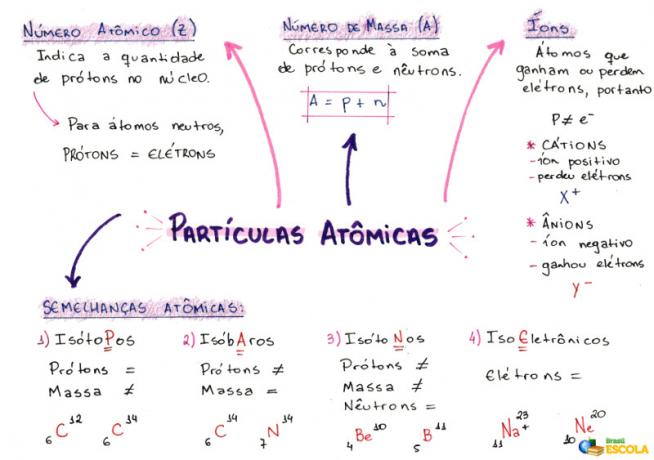
* Za preuzimanje mape uma u PDF-u, Kliknite ovdje!
Primjeri izračuna broja atomskih čestica
Primjer 1: Odrediti broj protona, neutrona i elektrona u atomu 14x29.
Dane su sljedeće vrijednosti za atom X:
Maseni broj (gore desno) = 29
Atomski broj (dolje lijevo) = 14
Da biste odredili broj protona:
Broj protona uvijek je jednak atomskom broju, pa X atom ima 14 protona.
Da biste odredili broj elektrona:
Kako atom X nije ion, stoga je broj elektrona jednak broju protona, odnosno 14.
Za određivanje broja neutrona:
Broj neutrona određuje se pomoću broja mase i protona u sljedećoj formuli:
A = p + n
29 = 14 + n
29 - 14 = n
n = 15
Primjer 2: Odrediti broj protona, neutrona i elektrona iona X+3, znajući da su njihov maseni broj odnosno atomski broj 51, odnosno 23.
Dane su sljedeće vrijednosti za ion X:
Maseni broj = 51
Atomski broj (dolje lijevo) = 23
Da biste odredili broj protona:
Broj protona uvijek je jednak atomskom broju, pa X atom ima 23 protona.
Da biste odredili broj elektrona:
Jon X je pozitivan (+3), pa je to kation koji je izgubio tri elektrona. Dakle, njegov broj elektrona je 20.
BILJEŠKA: Smanjenje ili povećanje broja elektrona uvijek se događa u odnosu na atomski broj.
Za određivanje broja neutrona:
Broj neutrona određuje se pomoću broja mase i protona u sljedećoj formuli:
A = p + n
51 = 23 + n
51 - 23 = n
n = 28
Primjer 3: Atom W ima atomski broj i masu jednaku, odnosno 29 i 57, što je izobare od a atom Y, koji ima atomski broj jednak 30, što je izotop atoma B, čiji je maseni broj 65. Pomoću ovih podataka odredite broj protona, neutrona i elektrona u atomu B.
Podaci dobiveni vježbom:
Atom W
atomski broj (dolje lijevo) = 29
maseni broj (gore desno) = 57
Y izobar, tj. Masa Y je također 57.
Y atom
atomski broj = 30
maseni broj = 57
S ove dvije vrijednosti moramo odrediti njegov neutronski broj jer je on izoton elementa B:
A = Z + n
57 = 30 + n
57 - 30 = n
n = 27
Atom B:
maseni broj = 65
broj neutrona = 27
S tim podacima moramo odrediti njegov atomski broj, jer ćemo time odrediti njegov broj protona i broj elektrona (jer to nije ion):
A = Z + n
65 = Z + 27
65 - 27 = Z
Z = 38
Prema tome, atom B ima 38 protona, 38 elektrona i 27 neutrona.
* Mind Map Victora Ricarda Ferreire
Učitelj kemije
Ja, Diogo Lopes Dias