एक प्रतिवर्ती प्रतिक्रिया यह तब होता है जब उत्पादों को वापस अभिकारकों में बदलना संभव होता है। इस तरह की प्रतिक्रिया आती है रासायनिक संतुलन जब प्रत्यक्ष प्रतिक्रिया के विकास की दर, यानी अभिकर्मकों की खपत और के गठन के साथ प्रतिक्रिया उत्पाद उसी गति से होते हैं जैसे रिवर्स रिएक्शन - अभिकारकों का निर्माण और उत्पादों की खपत।
इस प्रकार की संतुलित प्रतिक्रियाएँ दैनिक जीवन में बहुत अधिक देखने को मिलती हैं। एक उदाहरण है जो गुफाओं में होता है, तथाकथित स्टैलेक्टाइट्स और स्टैलेग्माइट्स के निर्माण में।
भूजल उच्च दबाव के अधीन है, इसलिए इसमें बड़ी मात्रा में कार्बन डाइऑक्साइड (CO .) होता है2(जी)) उसमें घुल गया। चूना पत्थर वाली मिट्टी से गुजरते समय (CaCO .)3(रों)), यह कार्बोनेट नीचे की प्रतिक्रिया के अनुसार घुल जाता है और गुफाएँ बन जाती हैं:
CaCO3(रों) + सीओ2(जी) + एच2हे(1) → सीए2+(यहां) + 2 एचसीओ-3 (एक्यू)
हालांकि, कार्बोनेट और कैल्शियम आयन प्रतिक्रिया कर सकते हैं, कैल्शियम कार्बोनेट के रूप में फिर से अवक्षेपित हो सकते हैं। यह प्रतिक्रिया द्वारा प्रदर्शित किया जाता है:
यहाँ2+(यहां) + 2 एचसीओ-3 (एक्यू)→ CaCO3(रों) + सीओ2(जी) + एच2हे(1)
जैसा कि आपने देखा होगा, एक प्रतिक्रिया दूसरे के ठीक विपरीत होती है: अभिकारक उत्पाद बन जाते हैं और उत्पाद अभिकारक बन जाते हैं। तो, हम इस प्रतिक्रिया को संतुलन में निम्नानुसार प्रस्तुत कर सकते हैं:
CaCO3(रों) + सीओ2(एक्यू) + एच2हे(1) यहाँ2+(यहां) + 2 एचसीओ-3 (एक्यू)
यहाँ2+(यहां) + 2 एचसीओ-3 (एक्यू)
गुफाओं की छत से खनिजयुक्त बूंदों से कार्बोनेट का धीमा और निरंतर फैलाव नीचे की ओर बहता है, उनका पानी वाष्पित हो जाता है और CO का विमोचन होता है।2. तो रासायनिक संतुलन विपरीत दिशा में (अभिकर्मकों के गठन के) स्थानांतरित हो जाता है, इसलिए CaCO3(रों) बनता है, अर्थात् stalactites गुफाओं की छत पर। गिरने पर, बूंद अभी भी कार्बोनेट को भंग कर देती है, जो गुफा के तल पर जमा हो जाती है, जिससे खनिज-स्तंभ निकलते.
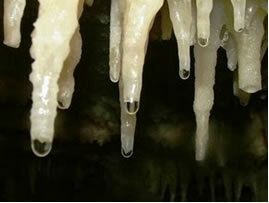
स्टैलेक्टाइट्स और स्टैलेग्माइट्स के निर्माण के लिए चूना पत्थर टपकने वाला पानी
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/equilibrio-quimico-nas-cavernas.htm
