NS पास्तापरमाणु, जैसा कि इसके नाम से पता चलता है, यह एक परमाणु का द्रव्यमान है, जिसे आमतौर पर "m ." द्वारा दर्शाया जाता हैNS"या" एमए "। हालांकि, चूंकि परमाणु एक अत्यंत छोटी इकाई है, जो मानव आंखों के लिए अदृश्य है, उदाहरण के लिए, तराजू का उपयोग करके इसके द्रव्यमान को मापना संभव नहीं है। इसलिए वैज्ञानिकों ने परमाणुओं के द्रव्यमान को अन्य परमाणुओं के द्रव्यमान से तुलना करके निर्धारित किया।
यह अन्य इकाइयों के साथ भी किया जाता है। उदाहरण के लिए, द्रव्यमान की इकाई मानक किलोग्राम है, जो 3.917 सेमी ऊंचाई और व्यास में एक सिलेंडर से मेल खाती है, जो 10% इरिडियम और 90% प्लैटिनम से बना है। तो यह एक तुलना के रूप में कार्य करता है। उदाहरण के लिए, यदि हम किसी वस्तु को पैमाने पर "वजन" करते हैं और हम पाते हैं कि उसका द्रव्यमान 10 किग्रा है, तो इसका अर्थ है कि उसका द्रव्यमान चुने हुए मानक से 10 गुना अधिक है: 1 किग्रा।
यही बात परमाणुओं पर भी लागू होती है। चुना गया मानक कार्बन -12 था, और इस परमाणु को मनमाने ढंग से 12 यू का द्रव्यमान सौंपा गया था। "यू" परमाणु द्रव्यमान की इकाई है और इसलिए कार्बन परमाणु के द्रव्यमान के 1/12 के बराबर है।
उदाहरण के लिए, जब हम कहते हैं कि हाइड्रोजन का परमाणु द्रव्यमान 1 u के बराबर है, तो इसका मतलब है कि यह ऐसा है जैसे यदि हम कार्बन को 12 भागों में विभाजित करते हैं, तो इनमें से किसी एक भाग का द्रव्यमान के परमाणु के द्रव्यमान के बराबर होता है हाइड्रोजन। एक अन्य उदाहरण सल्फर है, इसका परमाणु द्रव्यमान 32 u है, जिसका अर्थ है कि इसका द्रव्यमान इसके द्रव्यमान के 1/12 से 32 गुना अधिक है 12सी।
1 कार्बन परमाणु के द्रव्यमान का 1 u = 1/12 12

परमाणु द्रव्यमान इकाई कार्बन-12. का द्रव्यमान 1/12 है
पदार्थों का आणविक द्रव्यमान तत्वों के परमाणु द्रव्यमान का योग होता है। उदाहरण के लिए, ऑक्सीजन का परमाणु द्रव्यमान 16 u के बराबर है, इसलिए ऑक्सीजन गैस अणु का आणविक द्रव्यमान (O .)2) 32u के बराबर है।
चूंकि प्रयोगशाला तकनीकें वर्तमान में बहुत उन्नत हैं, ऐसे उपकरण हैं जो द्रव्यमान स्पेक्ट्रोमीटर जैसे तत्वों के परमाणु द्रव्यमान को सटीक रूप से मापते हैं। इस प्रकार, यह जानना संभव है कि 1 यू 1.66054 के बराबर है। 10-24 जी.
माइंड मैप: परमाणु द्रव्यमान
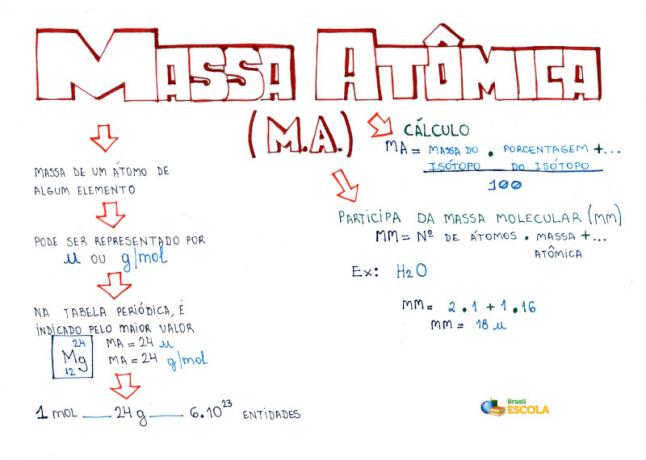
*मानसिक मानचित्र को PDF में डाउनलोड करने के लिए, यहां क्लिक करें!
चूँकि परमाणु द्रव्यमान बड़ी सटीकता के साथ निर्धारित किए जाते हैं, उन्हें आवर्त सारणी में दशमलव संख्याओं के रूप में दिया जाता है। लेकिन जब हम गणना करने जाते हैं, तो हम आमतौर पर गोल संख्या का उपयोग करते हैं, प्रयोगों के अपवाद के साथ जो बहुत सटीक होने की आवश्यकता होती है। उदाहरण के लिए, यदि आप आवर्त सारणी को देखते हैं, तो आप देखेंगे कि ऑक्सीजन का परमाणु द्रव्यमान 15,999 u के बराबर है, लेकिन हम आम तौर पर गणना में मान 16 u का उपयोग करते हैं। कार्बन के साथ भी ऐसा होता है, जिसका परमाणु द्रव्यमान 12.01 u है, जैसा कि नीचे दिखाया गया है:
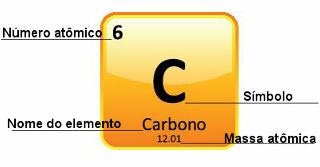
आवर्त सारणी में कार्बन का प्रतिनिधित्व
आवर्त सारणी में दिखाई देने वाले तत्व वास्तव में सभी तत्वों के प्राकृतिक समस्थानिकों का भारित औसत होते हैं। इस प्रकार, तालिका में दिखाई देने वाला परमाणु द्रव्यमान भी इन तत्वों के परमाणु द्रव्यमान का औसत है। उदाहरण के लिए, क्लोरीन (C?) के दो प्राकृतिक समस्थानिक हैं, 35 और 37, जिनकी प्रकृति में संबंधित प्रतिशत 75.76% और 24.24% हैं। इनमें से प्रत्येक समस्थानिक का परमाणु द्रव्यमान भिन्न होता है, जिसमें C?-35 का 34.96885 u और C का -37 का 36.96590 होता है।
इस तरह, तत्व के परमाणु द्रव्यमान की गणना प्रत्येक समस्थानिक के द्रव्यमान और प्रकृति में प्रकट होने वाली बहुतायत को ध्यान में रखकर की जाती है। क्लोरीन के मामले में, हमारे पास है:
क्लोरीन तत्व का परमाणु द्रव्यमान = (34,96885. 75,76%) + (36,96590. 24,24%)
100%
क्लोरीन तत्व का परमाणु द्रव्यमान = 35.45
यह आवर्त सारणी पर दिखाई देने वाले क्लोरीन का परमाणु द्रव्यमान मूल्य है।
* मेरे द्वारा माइंड मैप। डिओगो लोपेज
जेनिफर फोगाका द्वारा
पत्र में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-massa-atomica.htm