आप आक्साइड वे दो अलग-अलग तत्वों से बने होते हैं, जिनमें से एक ऑक्सीजन है, जिसे दोनों में से सबसे अधिक विद्युतीय होना चाहिए।
अकार्बनिक ऑक्साइड का नामकरण उन नियमों का पालन करता है जो इस बात पर निर्भर करते हैं कि ऑक्साइड आणविक, सहसंयोजक या आयनिक है या नहीं। आइए प्रत्येक मामले को देखें:
* आणविक आक्साइड या सहसंयोजक नेटवर्क का नामकरण:
आणविक या सहसंयोजक नेटवर्क ऑक्साइड वे होते हैं जिनमें ऑक्सीजन a. से जुड़ी होती है अधातु, जैसे कार्बन (सी), नाइट्रोजन (एन), सल्फर (एस), फ्लोरीन (एफ), दूसरों के बीच में। इन आक्साइडों का नामकरण निम्नलिखित नियम का पालन करता है:

अधातुओं से बनने वाले ऑक्साइडों के लिए नामकरण नियम
ऑक्सीजन से जुड़े तत्व के सामने मोनो उपसर्ग वैकल्पिक है।
उदाहरण के लिए, हमारे पास निम्नलिखित आणविक ऑक्साइड हैं: CO.
- ऑक्सीजन की मात्रा को इंगित करने वाला उपसर्ग: 1 ऑक्सीजन: मोनो;
- का ऑक्साइड;
- उपसर्ग जो दूसरे तत्व के परमाणुओं की संख्या को इंगित करता है: 1 कार्बन: मोनो;
- ऑक्सीजन से जुड़े तत्व का नाम: कार्बन.
तो आपका नाम इस प्रकार है: सीओ = मोनोकार्बन मोनोऑक्साइड या कार्बन मोनोऑक्साइड।
और उदाहरण देखें:
कार्बन डाइऑक्साइड - CO
2सल्फर ट्राइऑक्साइड - SO3
डाइक्लोरो हेप्टोक्साइड - Cl2हे7
डाइनाइट्रोजन मोनोऑक्साइड - N2हे
डाइनाइट्रोजन ट्राइऑक्साइड - N2हे3
नाइट्रोजन मोनोऑक्साइड -NO
नाइट्रोजन डाइऑक्साइड - NO2
डाइनाइट्रोजन पेंटोक्साइड - N2हे5
सिलिकॉन डाइऑक्साइड - SiO2
डिफोस्फोरस पेंटोक्साइड - पी2हे5
सल्फर ट्राइऑक्साइड - SO3
* आयनिक ऑक्साइड का नामकरण:
आयनिक ऑक्साइड वे होते हैं जिनमें ऑक्सीजन a. से बंधी होती है धातुजैसे लोहा (Fe), लेड (Pb), सोडियम (Na), कैल्शियम (Ca), सिल्वर (Ag), आदि। सामान्यतः ऑक्सीजन का विद्युत आवेश -2 होता है।
आणविक या सहसंयोजक नेटवर्क ऑक्साइड के लिए उल्लिखित नामकरण वर्तमान में धातु ऑक्साइड पर भी लागू होता है और इसे आधिकारिक माना जाता है. कुछ उदाहरण देखें:
आयरन मोनोऑक्साइड - FeO
लेड मोनोऑक्साइड - PbO
लेड डाइऑक्साइड - PbO2
विभिन्न ट्राइऑक्साइड - Fe2हे3
हालांकि, धातु आक्साइड के लिए एक विशिष्ट नामकरण है जो अभी भी व्यापक रूप से उपयोग किया जाता है। यह ऑक्सीजन से जुड़े तत्व की संयोजकता पर आधारित है।
यदि तत्व है एक एकल वैलेंस, अर्थात्, यदि ऑक्सीजन को बांधने और केवल एक प्रकार के ऑक्साइड बनाने का केवल एक ही तरीका है, तो नामकरण नियम द्वारा दिया जाएगा:

एकल-वैलेंट आयनिक ऑक्साइड नामकरण नियम
उदाहरण:
- सोडियम ऑक्साइड - Na2हे
- कैल्शियम ऑक्साइड - CaO
- पोटेशियम ऑक्साइड - K2हे
- एल्युमिनियम ऑक्साइड - Al2हे3
- सिल्वर ऑक्साइड - Ag2हे
लेकिन तत्वों द्वारा निर्मित आयनिक ऑक्साइड भी होते हैं एक से अधिक संयोजकता. इन मामलों में, नामकरण नियम इस प्रकार है:
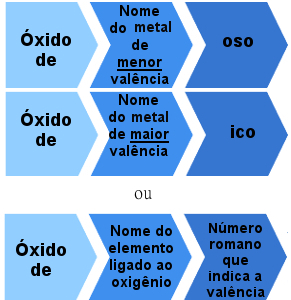
एक से अधिक संयोजकता वाले आयनिक ऑक्साइड के लिए नामकरण नियम rule
उदाहरण:
फेरस ऑक्साइड - FeO
फेरिक ऑक्साइड - Fe2हे3
क्यूप्रस ऑक्साइड - Cu2हे
कप्रिक ऑक्साइड - CuO
या:
आयरन ऑक्साइड II - FeO (आयरन नॉक्स = +2)
आयरन ऑक्साइड III - Fe2हे3 (आयरन नॉक्स = +3)।
कॉपर ऑक्साइड I - Cu2हे (आयरन नोक्स = +1)
कॉपर ऑक्साइड II - CuO (आयरन नोक्स = +2)।
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/nomenclatura-dos-oxidos.htm