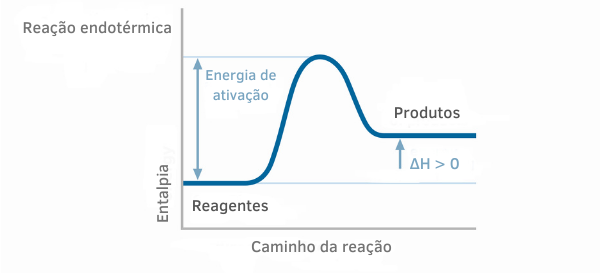
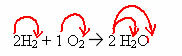Entropie c'est la mesure du degré de désordre d'un système, étant une mesure de l'indisponibilité de l'énergie.
C'est une grandeur physique qui est liée à Deuxième loi de la thermodynamique et qu'elle tend à augmenter naturellement dans l'Univers.
Définition de l'entropie
Le « désordre » ne doit pas être compris comme un « désordre », mais plutôt comme une forme d'organisation du système.
Le concept d'entropie est parfois appliqué dans d'autres domaines de la connaissance avec ce sens du désordre, plus proche du sens commun.
Par exemple, imaginons trois pots, un avec des petites billes bleues, un autre avec le même type de billes mais rouges, et le troisième vide.
On prend le pot vide et on met toutes les boules bleues dessous et toutes les boules rouges dessus. Dans ce cas, les boules sont séparées et organisées par couleur.
En secouant le pot, les billes ont commencé à se mélanger de telle sorte qu'à un moment donné il n'y a plus la séparation initiale.
Même si on continue à secouer la marmite, il est peu probable que les boules reviennent à la même organisation initiale. C'est-à-dire que le système ordonné (boules séparées par la couleur) est devenu un système désordonné (boules mélangées).

Ainsi, la tendance naturelle est d'augmenter le désordre d'un système, ce qui signifie une augmentation de l'entropie. On peut alors dire que dans les systèmes: ΔS >0, où S est l'entropie.
Comprenez aussi ce que c'est enthalpie.
Entropie et thermodynamique
Le concept d'Entropie a commencé à être développé par l'ingénieur et chercheur français Nicolas Sadi Carnot.
Dans ses recherches sur la transformation de l'énergie mécanique en thermique, et vice versa, il a constaté qu'il serait impossible qu'il y ait une machine thermique pleinement efficace.
LES Première loi de la thermodynamique détermine essentiellement que "l'énergie est conservée". Cela signifie que dans les processus physiques, l'énergie n'est pas perdue, elle est convertie d'un type à un autre.
Par exemple, une machine utilise de l'énergie pour effectuer un travail et, dans ce processus, la machine se réchauffe. C'est-à-dire que l'énergie mécanique est dégradée en énergie thermique.
L'énergie thermique ne se transforme pas en énergie mécanique (si cela se produisait, la machine ne planterait jamais), le processus est donc irréversible.
Plus tard, Lord Kelvin complète les recherches de Carnot sur l'irréversibilité des processus thermodynamiques, donnant naissance aux fondements de Deuxième loi de la thermodynamique.
Rudolf Clausius a été le premier à utiliser le terme Entropie en 1865. L'entropie serait la mesure de la quantité de L'énérgie thermique qui ne peut pas être inversée en énergie mécanique (ne peut pas faire de travail) à une certaine température.
Clausius a développé la formule mathématique pour la variation de l'entropie ()S) qui est actuellement utilisée.
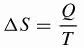
Étant,
ΔS: variation d'entropie (J/K)
Q: chaleur transférée (J)
T: température (K)
Lire aussi:
- Thermodynamique
- Cycle Carnot
- Énergie
- Types d'énergie
- Formules de physique
Exercices résolus
1) Enem - 2016
Jusqu'en 1824, on croyait que les moteurs thermiques, dont les moteurs à vapeur et les moteurs à combustion actuels, pouvaient avoir un fonctionnement idéal. Sadi Carnot a démontré l'impossibilité d'une machine thermique, fonctionnant en cycles entre deux sources thermiques (une chaude et une froide), pour obtenir un rendement de 100 %. Une telle limitation se produit parce que ces machines
a) effectuer des travaux mécaniques.
b) produire une entropie accrue.
c) utiliser des transformations adiabatiques.
d) contrevenir à la loi de conservation de l'énergie.
e) fonctionner à la même température que la source chaude.
Alternative: b) produire une entropie accrue.
2) Enem - 2011
Un moteur ne peut fonctionner que s'il reçoit une quantité d'énergie d'un autre système. Dans ce cas, l'énergie stockée dans le combustible est en partie libérée lors de la combustion pour que l'appareil puisse fonctionner. Lorsque le moteur tourne, une partie de l'énergie convertie ou transformée en combustion ne peut pas être utilisée pour faire du travail. Cela signifie qu'il y a une fuite d'énergie sous une autre forme. Carvalho, A. X. Z.
Physique Thermique. Belo Horizonte: Pax, 2009 (adapté).
Selon le texte, les transformations d'énergie qui se produisent pendant le fonctionnement du moteur sont dues à une
a) le dégagement de chaleur à l'intérieur du moteur est impossible.
b) le travail effectué par le moteur est incontrôlable.
c) la conversion complète de la chaleur en travail est impossible.
d) la transformation de l'énergie thermique en cinétique est impossible.
e) la consommation potentielle d'énergie du combustible est incontrôlable.
Alternative: c) la conversion complète de la chaleur en travail est impossible.
Voir aussi: Exercices sur la thermodynamique