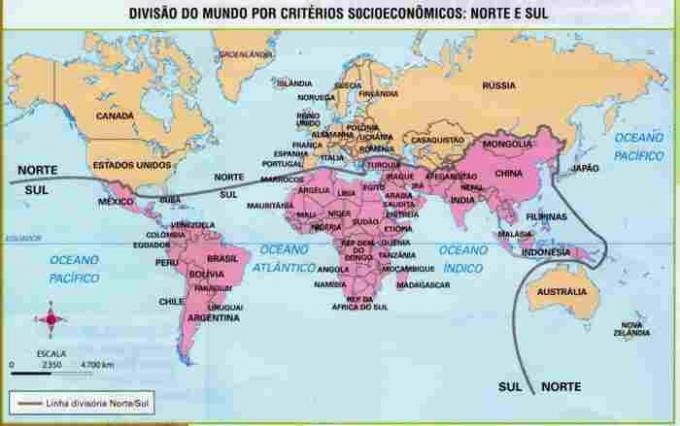
Toi esters sont des composés organiques oxygénés formés par la réaction chimique entre un acide carboxylique c'est un de l'alcool. Présenter le groupe fonctionnel (composé de deux atomes d'oxygène et de deux radicaux R) représenté ci-dessous :
Groupe fonctionnel général d'un ester
Structurellement, ce qui caractérise le ester c'est la présence d'un radical alkyle lié directement à l'atome d'oxygène. Dans ce cas, le radical (R) attaché au carbone – qui, à son tour, est doublement attaché à l'oxygène – peut être soit un radical alkyle, soit un atome d'hydrogène.
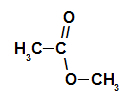
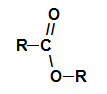
Chaîne carbonique d'un ester
réaction d'estérification
il s'agit de la réaction chimique qui produit un ester et une molécule d'eau à partir de l'interaction entre un acide carboxylique et un alcool, comme dans l'équation ci-dessous :
Équation chimique représentant la formation d'un ester
Au cours de l'estérification, le groupe hydroxyle (OH) de l'alcool interagit avec le hydrogène (H) ionisable de l'hydroxyle de l'acide et forme le molécule d'eau.
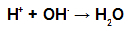
Molécule d'eau formant des groupes dans l'estérification
déjà le ester il est formé en liant le radical (R) de l'alcool à l'oxygène, qui reste de l'hydroxyle de l'acide après la formation d'eau.
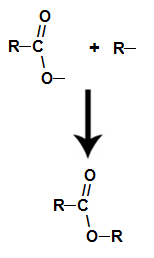
Formation de la molécule d'ester
Caractéristiques des esters
Principales propriétés physiques présentées par esters:
Ils ont des arômes de fruits et de fleurs ;
bas esters masse molaire ils sont liquides à température ambiante et ceux de masse molaire élevée sont solides ;
Comparés aux alcools et aux acides carboxyliques, les esters ont des points de fusion et d'ébullition inférieurs ;
Par rapport à l'eau, les esters de masse molaire inférieure sont moins denses;
Les esters de masse molaire inférieure sont polaires et ceux de masse molaire supérieure sont non polaires ;
Dans les esters polaires, les forces prédominent dipôle permanent; dans le non polaire, les forces prédominent dipôle induit;
Les esters de masse molaire inférieure sont peu solubles dans l'eau et ceux de masse plus élevée sont insolubles dans l'eau.
Une règle de nommage des esters
Avant d'utiliser la règle de nommage d'un ester, il est essentiel de rappeler que ce composé est formé par l'union de deux parties, l'une provenant de d'acide carboxylique (en rouge) et l'autre d'alcool (en bleu), comme représenté par l'image a poursuivre:
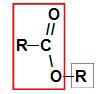
Identification des parties à l'origine de l'ester
Selon l'Union internationale de chimie pure et appliquée (UICPA), la règle officielle pour nommer un ester est :
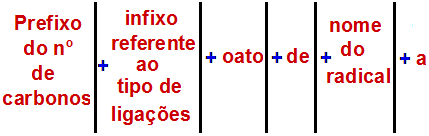
Une règle de nommage des esters
Noter: Le préfixe et l'infixe correspondent toujours à la partie acide carboxylique, et le radical correspond à la partie alcool.
Voir ci-dessous quelques exemples d'application de la règle de nommage des esters :
1er exemple: essence de framboise
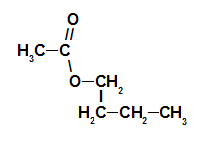
Formule développée de l'ester d'essence de framboise
Pour nommer cet ester, on utilise :
N° PréfixeO de carbones: et, puisque l'acide formant a deux carbones;
Infixe sur le type de liens: un, car l'acide formant n'a que des liaisons simples entre les carbones ;
l'acte;
dans;
Radical: butyle, en ayant quatre carbones en séquence ;
le.
Ainsi, le nom de l'ester correspondant à l'essence de framboise est éthanolate de butyle.
2e exemple : essence de pomme de pin
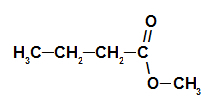
Formule développée de l'ester de pomme de pin
Pour former le nom de cet ester, on utilise :
N° PréfixeO de carbones: mais, puisque l'acide formant a quatre carbones;
Infixe sur le type de liens : un, car l'acide formant n'a que des liaisons simples entre les carbones ;
l'acte;
dans;
Radical: méthyle, car l'alcool de formation n'a qu'un seul carbone ;
le.
Ainsi, le nom de l'ester correspondant à l'essence de pomme de pin est butanoate de méthyle.
3ème exemple : essence de fraise
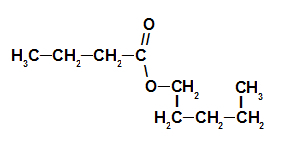
Formule structurelle d'ester d'essence de fraise
Pour nommer cet ester, on utilise :
N° PréfixeO de carbones : mais, puisque l'acide formant a quatre carbones;
Infixe sur le type de liens: un, car l'acide formant n'a que des liaisons simples entre les carbones ;
l'acte;
dans;
Radical: pentyle, car l'alcool de formation a cinq atomes de carbone en séquence;
le.
Ainsi, le nom de l'ester correspondant à l'essence de fraise est butanoate de pentyle.
Utilisations des esters
Les esters sont bien connus pour leur utilisation comme arôme dans les aliments transformés, c'est-à-dire les substances qui simulent la saveur et l'arôme caractéristiques des aliments naturels, tels que les fruits. Par ailleurs, les esters sont encore utilisés dans la fabrication de médicaments, de cosmétiques, de parfums et de cires.
Par moi Diogo Lopes Dias
La source: École du Brésil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ester.htm