La capacité qu'ont les connexions à attirer des charges électriques est définie comme la Polarité, qui prend un caractère différent selon la connexion où elle est présente.
Les liaisons les plus fréquentes impliquant des composés organiques se produisent entre atomes de carbone ou entre atomes de carbone et d'hydrogène: C C et C ─ H (hydrocarbures). Nous classons ce type de liaison comme covalente, elle est présente dans toutes les liaisons de composés organiques formées uniquement par le carbone et l'hydrogène.
Lorsque dans la molécule d'un composé organique il y a un autre élément chimique en plus du carbone et de l'hydrogène, ses molécules auront une certaine polarité. Nous appelons cet élément un hétéroatome et il peut s'agir de: azote (N), oxygène (O), entre autres.
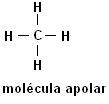
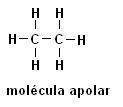
Méthane (CH4) Éthane (C2H6)
Notez que dans les deux structures, il n'y a pas de présence d'hétéroatomes, dans ce cas les molécules sont classées comme non polaires.


La présence d'oxygène en tant qu'hétéroatome fait que les molécules montrent une polarité. La première molécule est le composé Ethanol (
CH3CH2Oh), la présence d'hydroxyle – OH confère à ce composé un caractère polaire, même si dans sa structure il contient une partie apolaire.Par Líria Alves
Diplômé en Chimie
Équipe scolaire du Brésil
Voir plus! isomère plat
Chimie organique - Chimie - École du Brésil
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/moleculas-organicas-polares-apolares.htm
