O chlorure de vinyle c'est un hydrocarbure action chlorée toxique et cancérigène. C'est un gaz incolore à température ambiante, hautement inflammable et sensible à la chaleur.
C'est le monomère utilisé dans la fabrication du chlorure de polyvinyle, une substance connue sous le nom de PVC. O PVC est un thermoplastique résistant à la chaleur (contrairement à son monomère) qui a de nombreuses applications dans le vie quotidienne, comme le revêtement de fils électriques, la construction de tuyaux et divers types de emballage.
A lire aussi :Amiante - fibre naturelle avec une large application industrielle, mais extrêmement toxique pour l'homme
Résumé sur le chlorure de vinyle
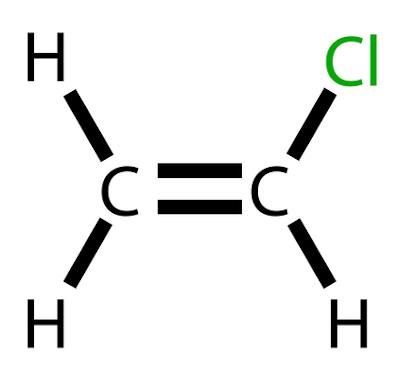
Le chlorure de vinyle est un hydrocarbure chloré de formule H2C=CHCl.
C'est un gaz incolore, odorant et hautement inflammable.
Le chlorure de vinyle est instable chaleur, en cours de décomposition.
La principale application du chlorure de vinyle est la fabrication de chlorure de polyvinyle (PVC).
Le PVC est un thermoplastique avec de nombreuses applications, telles que la tuyauterie, les pièces, les revêtements, les emballages, etc.
Le chlorure de vinyle est toxique et a un effet cancérigène.
propriétés du chlorure de vinyle
formule moléculaire: CH2CH Cl (C2H3Cl).
Masse moléculaire: 62,498 g/mol.
état physique: gaz (incolore et à forte odeur).
Densité: 0,91 g/ml.
Solubilité dans l'eau: très légèrement soluble (0,6 g dans 100 mL d'eau, 20 °C).
température de fusion: -154°C.
Température d'ébullition : -13°C.
Qu'est-ce que le chlorure de vinyle ?
Le chlorure de vinyle est un hydrocarbure chloré de formule H2C=CHCl. A température ambiante, il se produit avec un Gaz incolore et hautement inflammable.
Le chlorure de vinyle, également appelé chloroéthène ou monomère de chlorure de vinyle, est un produit chimique de grande importance dans industrie, ayant une application spéciale dans la fabrication de polymère chlorure de polyvinyle, plus connu sous le nom de PVC. Ce composé occupe la liste des 20 produits dérivés de Pétrole d'une plus grande pertinence industrielle et économique.
A lire aussi :Benzopyrène — hydrocarbure cancérigène présent dans la fumée de cigarette et les viandes grillées
Caractéristiques du chlorure de vinyle
Le chlorure de vinyle est un Gaz incolore à odeur douce et sucrée. Il a la propriété d'être hautement inflammable.
En cas d'exposition à des sources de chaleur, peut se décomposer en dégageant des vapeurs toxiques dans gaz carbonique, monoxyde de carbone, chlorure d'hydrogène et phosgène. Parce qu'il s'agit d'un composé organique, sa solubilité dans l'eau est extrêmement faible, par contre il est soluble dans des substances telles que éthanol, benzène et le tétrachlorure de carbone.
En présence d'humidité, le chlorure de vinyle devient corrosif et peut attaquer les fer et le acier. Il a la capacité de polymériser lorsqu'il est exposé à la chaleur de l'air atmosphérique, par une réaction exothermique. Cette propriété tire bon nombre de ses applications industrielles.
Le chlorure de vinyle demande de l'attention car il est toxique et cancérigène.
A quoi sert le chlorure de vinyle ?
Le chlorure de vinyle est le monomère utilisé pour fabriquer le polymère PVC (chlorure de polyvinyle) et autres solvants chlorés.
Le PVC est un thermoplastique utilisé dans la fabrication d'emballages, de chaussures, de connexions électriques et de câbles, tuyaux, fenêtres, tubes et sacs de prélèvement sanguin, vêtements, parmi d'innombrables autres articles.

O Le PVC est formé par la polymérisation du chlorure de vinyle. Dans ce processus chimique, un grand nombre de molécules de chlorure de vinyle s'ajoutent les unes aux autres, formant une grande structure chimique.
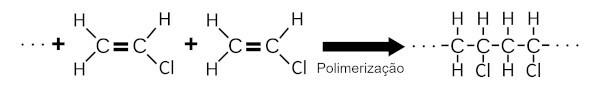
O Le PVC est ignifuge et pour cette raison, il est largement utilisé dans le revêtement des fils, des câbles électriques et des revêtements résidentiels.
Bien que le chlorure de vinyle soit un composé chimique qui demande de l'attention en raison de sa toxicité et instabilité thermique, son polymère PVC est très stable aux sources de chaleur, il est non toxique et peut être stocké Avec la sécurité.
Jusqu'en 1974, le chlorure de vinyle était utilisé dans les aérosols. Dans le passé, il était même utilisé comme anesthésique par inhalation. Connaissant la toxicité de ce composé, ces applications ont été abandonnées.
Obtention du chlorure de vinyle
La synthèse du chlorure de vinyle utilisé à l'échelle industrielle est initié avec le composé éthylène ou éthène (CH2=CH2) et peut se produire par deux voies.
Dans le premier, l'éthylène est converti en 1,2-dichloroéthane par réaction avec le chlore gazeux. Ensuite, en chauffant le 1,2-dichloroéthane en présence d'un catalyseur, on obtient le chlorure de vinyle comme produit principal et le acide hydrochlorique comme produit secondaire.
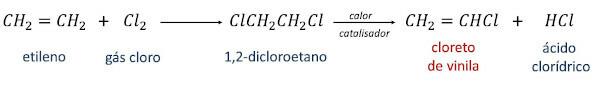
Dans la deuxième voie de réaction, appelée oxychloration, la réaction entre l'éthylène, l'acide chlorhydrique et oxygène de l'atmosphère elle-même, en présence de chaleur et d'un catalyseur, générant du chlorure de vinyle et de l'eau comme produits.

En règle générale, un centre de fabrication de chlorure de vinyle est construit pour accueillir les deux processus de fabrication. cité, de sorte que l'acide chlorhydrique généré dans la première méthode agit comme un réactif pour la réalisation de la seconde itinéraire.
Précautions avec le chlorure de vinyle
Le chlorure de vinyle est un composé toxique. Comme c'est un gaz, La principale forme de contamination est par inhalation., c'est pourquoi sa manipulation doit toujours être effectuée à l'aide d'équipements appropriés, tels que des masques à gaz.
L'exposition à cette substance affecte système nerveux périphérique et central, causant des dommages à la foie. UN Une exposition continue peut déclencher le phénomène de Raynaud, qui est un ensemble de symptômes qui incluent des douleurs articulaires et musculaires et des changements cutanés, qui peuvent évoluer vers une perte complète d'élasticité de la peau, affectant même organes organes internes et vaisseaux sanguins.
D'autres effets comprennent l'euphorie, la désorientation, les fausses couches et les malformations congénitales. Les blessures au tissu oculaire sont également enregistrées.
Les symptômes dépendent du niveau d'exposition à la substance, allant de vertiges, nausées, troubles visuels, maux de tête et ataxie en cas d'exposition aiguë (de 1000 à 8000 ppm de chlorure de vinyle dans l'air), à effet narcotique, arythmie cardiaque et insuffisance respiratoire mortelle en cas d'exposition à des niveaux supérieurs à 12000 ppm.
Chlorure de vinyle et cancer
O le chlorure de vinyle est une substance cancérigène, associée à un risque élevé de développer un cancer du foie, ce qui peut contribuer à la survenue de cancer du cerveau et du poumon, ainsi que le cancer du système lymphatique.
A lire aussi :Nitrate d'ammonium - composé utilisé en agriculture qui peut provoquer des explosions
Présence de chlorure de vinyle
le chlorure de vinyle est généré spontanément dans l'environnement par la décomposition de certains composés contenant chloregrâce à l'action des micro-organismes. Par conséquent, il peut être considéré comme un contaminant de l'air et de l'eau, en particulier dans les régions proches de décharges.
Cependant, l'occurrence la plus élevée de chlorure de vinyle se fait par des voies de synthèse, liées à l'industrie chimique, comme indiqué précédemment.
Histoire du chlorure de vinyle
Le chlorure de vinyle était découverte en 1835 par le chimiste allemand Justus von Liebig, lors de la réaction du dichloroéthane avec de l'hydroxyde de potassium dans un environnement alcoolique.
Plus tard, en 1872, le chimiste Eugen Baumann a observé pour la première fois la polymérisation du chlorure de vinyle, à l'origine du PVC, après avoir laissé un récipient avec la substance exposée au soleil par accident.
En 1926, l'inventeur américain Waldo Semon a découvert des additifs chimiques qui conféraient une plus grande élasticité et malléabilité au PVC, élargissant les possibilités d'application de cette substance. Vers 1950, le PVC a commencé à être utilisé à l'échelle industrielle. Actuellement, le PVC est l'un des thermoplastiques les plus utilisés au monde.
Par Ana Luiza Lorenzen Lima
Professeur de chimie
Source: École du Brésil - https://brasilescola.uol.com.br/quimica/cloreto-de-vinila.htm
