La matière peut subir deux principaux types de transformations, physiques et chimiques. La transformation physique se produit lorsque la nature de la matière n'est pas modifiée, c'est-à-dire sa composition. Par exemple, quand on coupait un morceau de bois, il subissait une transformation, mais c'était un phénomène physique, car c'est encore du bois, sa constitution est la même qu'à l'origine.
D'autre part, une transformation ou un phénomène chimique se produit lorsque la nature ou la composition de la matière est modifiée. Dans ce cas, les particules initiales (qui peuvent être des molécules, des atomes, des amas ioniques, des ions, etc.) sont comme désassemblés et leurs atomes se réarrangent, assemblant de nouvelles molécules, amas, atomes, ions, etc., c'est-à-dire de nouveaux substances. C'est un réaction chimique.
Par exemple, imaginez que nous apportions une allumette allumée près de l'alcool éthylique. Nous savons ce qui va se passer: l'alcool va commencer à brûler. Cela signifie qu'il subit une réaction chimique avec l'oxygène de l'air (O
2) et changera de composition, n'étant plus de l'éthanol (C2H6O), et l'oxygène n'aura plus non plus sa composition initiale, à l'origine de nouvelles substances, qui sont le dioxyde de carbone (CO2) et de l'eau (H2O).
Alcool en feu - réaction de combustion
Dans les réactions chimiques, les substances initiales sont appelées réactifs et la fin de des produits, et les réactions sont représentées par équations chimiques, qui suivent la structure générale suivante :
RÉACTIFS → PRODUITS
En considérant l'exemple précédent de la réaction de combustion complète de l'alcool (éthanol), on a l'équation chimique suivante :
Éthanol + oxygène gazeux → dioxyde de carbone + eau
Cette réaction chimique est représentée ci-dessous au moyen d'atomes selon le modèle de Dalton, sous forme de sphères simples :
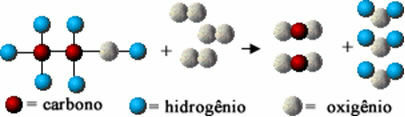
Représentation modèle d'une réaction de combustion d'éthanol
Notez que les liaisons initiales entre les atomes ont été rompues et qu'ils ont formé de nouvelles liaisons, et de nouvelles substances sont apparues.
Ainsi, les équations chimiques sont écrites à l'aide de formules et de symboles qui représentent le mieux le schéma ci-dessus. Dans le cas considéré (réaction de combustion de l'éthanol), on a que l'équation chimique s'exprime comme suit :
Ç2H5Oh(?) + 3O2(g) → 2 CO2(g) + 3H2O(v)
Certains facteurs visuels indiquent qu'il y a eu une réaction chimique, à savoir :
* Libération de gaz;
* Changement de couleur;
* Formation de précipités;
* Apparition de flamme ou de luminosité.
Les processus importants qui se produisent dans notre corps, dans la nature et dans les industries, tels que la production de médicaments et d'aliments industrialisés, sont des réactions chimiques. Par conséquent, ils sont extrêmement importants pour l'émergence et le maintien de la vie.
Il existe plusieurs types de réactions chimiques, que l'on peut classer selon divers critères, mais les principaux types étudiés en chimie sont :
1. Réactions inorganiques : Ils sont généralement classés selon le nombre de substances formées, le nombre de réactifs et la présence ou l'absence de substances simples et composées. Il existe quatre principaux types de réactions inorganiques :
1.1. Réactions de synthèse ou d'addition;
1.2. Réaction de décomposition ou d'analyse;
1.3. Echange simple, déplacement ou réaction redox;
1.4. Double échange ou réaction de métathèse;
2. Réactions organiques : Ce sont ceux qui impliquent des composés carbonés. Ils sont généralement classés en trois grands types :
2.1. Réactions d'addition;
2.2. Réactions de remplacement;
2.3. Réactions d'élimination.
Par Jennifer Fogaça
Diplômé en Chimie
La source: École du Brésil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-reacao-quimica.htm