Comme expliqué dans le texte États physiques de l'eau et ses changements, le passage du solide au liquide est appelé La fusion. En conséquence,le point de fusion est la température à laquelle une substance pure qui était à l'état solide passe à l'état liquide.
Si vous prenez un glaçon qui était au réfrigérateur à une température de -5°C et que vous le laissez dehors par une journée chaude, que se passera-t-il? C'est simple, le glaçon va commencer à fondre. Mais cela n'arrivera qu'après l'avoir sorti du réfrigérateur. C'est parce que la température de la glace commence à augmenter, passant de -5 ºC à -4 ºC, puis à -3 ºC et ainsi de suite jusqu'à ce qu'elle atteigne 0 ºC. C'est la température à laquelle la glace commence à fondre. On peut donc dire que le point de fusion ou la température de fusion de la glace est égal à 0°C (au niveau de la mer).
*Rappelez-vous que ºC signifie degré Celsius, qui est une mesure de la température.

faire fondre la glace ou fondre
La chose la plus intéressante est que la température reste à la même valeur tout au long du changement d'état physique. Cela signifie que, dans le cas de la glace, après avoir atteint le point de fusion, sa température reste fixée à 0 °C jusqu'à ce que toute la glace passe à l'état liquide.
Cela peut être visualisé dans un graphique comme celui ci-dessous. A noter que, jusqu'à atteindre la température de fusion, la température a continué d'augmenter, mais lorsque cette température a été atteinte, elle est restée fixe dans le temps, formant un plateau :

Graphique du point de fusion de la glace
Le point d'ébullition est la température à laquelle une substance pure passe d'un état liquide à un état vapeur. C'est ce qui arrive quand on met l'eau liquide qui sort du robinet dans le feu. Sa température augmente jusqu'à atteindre une température de 100ºC, qui est le point d'ébullition de l'eau (au niveau de la mer).
Dans la figure suivante, vous pouvez voir que lorsque le liquide est chauffé, une augmentation de l'agitation se produit. de ses particules, ce qui leur permet de s'échapper du récipient et de se mélanger à l'air. Les bulles formées à la température d'ébullition sont des bulles de vapeur d'eau.
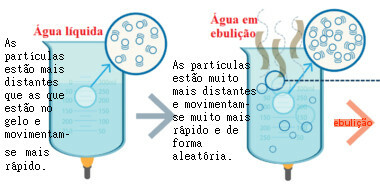
Mouvement des particules d'eau bouillante
Au point d'ébullition, il se passe la même chose qu'au point de fusion, c'est-à-dire que la température reste à la même valeur pendant le changement d'état.
Le graphique suivant montre le point de fusion (MP) et le point d'ébullition (PE) de l'eau :

Graphique de changement d'état physique de l'eau au niveau de la mer
Les points de fusion et d'ébullition sont des propriétés importantes des substances, car chacun a une température de fusion et une température d'ébullition spécifiques. Il n'y a pas deux substances ou plus avec les mêmes points de fusion et d'ébullition. La seule substance connue avec un point de fusion de 0°C et un point d'ébullition de 100°C au niveau de la mer est l'eau.
Par conséquent, ces quantités sont utilisées pour identifier les substances. Voir quelques valeurs de point de fusion et d'ébullition pour d'autres substances :

Points de fusion et d'ébullition de certains matériaux présents dans la vie quotidienne
Cependant, il est à noter que les températures de fusion et d'ébullition n'auront des valeurs fixes que si la substance est pure. Dans le cas des mélanges, ces valeurs varient, c'est-à-dire qu'elles bout à une température et finissent par changer d'état physique à une autre. Ainsi, les graphiques d'évolution de l'état physique des mélanges n'ont pas ces deux seuils fixes pour le point de fusion et pour le point d'ébullition.
Par Jennifer Fogaça
Diplômé en Chimie