Avez-vous déjà essayé de laver la vaisselle en utilisant uniquement de l'eau ?─ Ça ne marche pas, n'est-ce pas ?!Pourquoi l'eau seule ne peut-elle pas éliminer la graisse et la saleté ?Cette cela se produit parce que la composition de ces matériaux est très différente de la composition de l'eau, ce qui rend difficile leur mélange.
On dit que les molécules d'eau sont polaire, c'est-à-dire qu'ils ont des parties chargées: une partie est positive et l'autre est négative.Les graisses et les huiles sont apolaire, ce qui signifie que ses molécules n'ont pas de charge.Ainsi, les molécules polaires d'eau ne peuvent pas pénétrer dans les molécules de graisse et les entraîner. C'est pour cette même raison que l'huile ne se mélange pas à l'eau, comme le montre la figure suivante :

L'eau et l'huile ne se mélangent pas car l'eau est polaire et l'huile non polaire
Un autre problème est que les molécules d'eau forment une sorte de « peau » ou de « film » qui rend encore plus difficile la pénétration de la saleté. Cette couche mince est appelée la tension superficielle de l'eau. Sa formation se produit parce que la partie positive d'une molécule d'eau attire la partie négative d'une autre molécule d'eau, et ainsi de suite.
De cette façon, les molécules sont très proches les unes des autres, en particulier les molécules de surface, formant le film dont nous parlons. L'illustration suivante montre comment les molécules d'eau (symbolisées par les boules bleues) s'attirent et créent une tension superficielle :
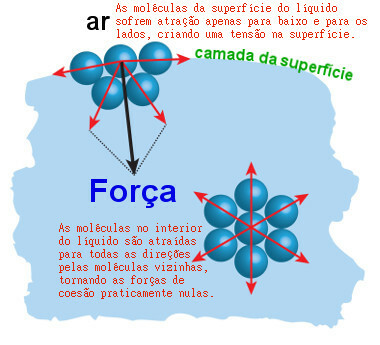
La tension superficielle est un "film" formé par les forces d'attraction entre les molécules d'eau de surface
La preuve que l'eau a réellement ce "film" est montrée dans l'image ci-dessous, dans laquelle un insecte peut marcher sur l'eau :

Insecte sur l'eau en raison d'une tension superficielle intense
Donc, pour pouvoir nettoyer la graisse et la saleté, nous devons utiliser du savon.Mais comment fonctionne le savon? Comment ça nettoie ?
Essentiellement, le savon est capable de « casser » ce « film » d'eau, lui permettant de pénétrer les matériaux et d'éliminer la saleté. C'est pourquoi le savon est souvent appelé un tensioactif ou alors tensioactif, parce qu'il diminue la tension superficielle de l'eau. C'est comme si le savon rendait l'eau « plus humide », tu sais ?!
Mais comment l'obtient-il ?Pour comprendre, regardez l'image ci-dessous qui montre la structure d'un savon :
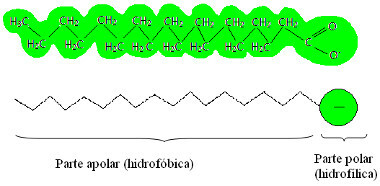
Structure typique d'un savon
Assurez-vous que le savon a une partie non polaire (ainsi que la graisse et l'huile)et une autre partie polaire (tout comme l'eau).De cette façon, la partie non polaire de la molécule de savon interagit avec les molécules non polaires des graisses et des huiles,et la partie polaire interagit avec les molécules polaires de l'eau.
Les molécules de savon se répartissent et forment des micelles, comme le montre la figure suivante :
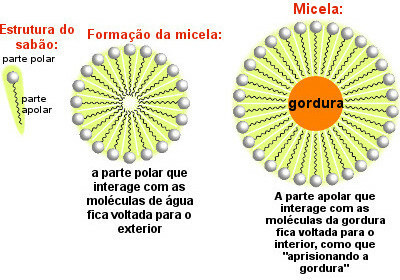
Savon Mixen Wrapping Graisse
Notez que la partie non polaire des molécules de savon entoure la particule de graisse, qui est entraînée par l'eau qui est en contact avec la partie polaire du savon tournée vers l'extérieur. Ainsi, les micelles formées par le savon aident à éliminer les salissures grasses.
Par Jennifer Fogaça
Diplômé en Chimie