Harkitse alla olevaa yleistä palautuvaa reaktiota, jossa pienet kirjaimet vastaavat tasapainotettuja reaktiokertoimia ja isot kirjaimet ovat reagoivia aineita ja kaikki tuotteet ovat kaasumaisia:

Tarkasteltaessa kutakin reaktion suuntaa erikseen, niiden kehitysnopeudet (Td) saadaan seuraavasti:
* Suora reaktio: aA + bB → cC + dD
Kaikkisuoraan = Ksuoraan. [THE]. [B]B
* Käänteinen reaktio: cC + dD → aA + bB
Kaikkikäänteinen = Kkäänteinen. [Ç]ç. [D]d
Kemiallisen tasapainovakion pitoisuus aineen määrässä (Kç) ja osapaineessa (KP) saadaan jakamalla Ksuoraan kirjoittanut Kkäänteinen.
Joten meillä on:
Ksuoraan. [THE]. [B]B = 1 → Ksuoraan__ = __[Ç]ç. [D]d___
Kkäänteinen. [Ç]ç. [D]d Kkäänteinen [THE]. [B]B
Oleminen, K.ç =_Ksuoraan_
Kkäänteinen
Joten meillä on:
Kç =__[Ç]ç. [D]d___ tai K.P =__(Praça)ç. (pD)d___ |
Missä p on kunkin aineen osapaine tasapainossa.
Tällä tavoin kukin pitoisuus nostetaan eksponentiksi, joka vastaa vastaavan aineen kerrointa reaktiossa, ja Kç ei ole yksikköä *.
Lisäksi erittäin tärkeä näkökohta on korostettava tässä lausekkeessakiinteitä komponentteja tai puhtaita nesteitä ei tulisi edustaa., koska vain ne seikat, jotka voivat kärsiä vaihteluista, osallistuvat tähän ilmaisuun. Kiinteässä tilassa olevan aineen pitoisuus aineen määrässä on vakio ja sisältyy siten jo itse K: n arvoon.ç. Sama koskee puhtaita nesteitä, kuten vettä. Lyhyesti, vain kaasumaisessa tilassa ja vesiliuoksessa olevat aineet osallistuvat ilmentymiseen.
Huomaa alla olevat esimerkit:
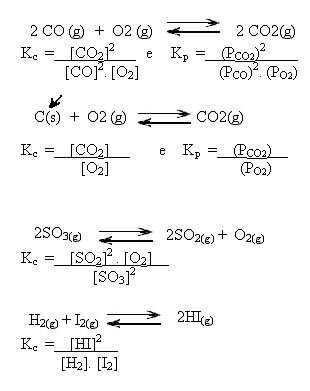
K-arvotç voi osoittaa meille, onko reagoivien aineiden ja tuotteiden pitoisuus sama tai onko toinen suurempi kuin toinen:
- jos Kç tai K.P on yhtä kuin yksi (Kç = 1), tämä tarkoittaa, että reagenssien ja tuotteiden pitoisuus on sama;
- jos arvo Kç tai K.P ole pitkä, tämä tarkoittaa, että tuotteiden pitoisuus on suurempi, koska K: n ilmentämisessäç tuotteet ovat osoittajassa;
- jos arvo Kç tai K.P on matala, tämä tarkoittaa, että reagenssit ovat suuremmissa pitoisuuksissa, koska K: n ilmentämisessäç reagenssit ovat nimittäjässä.
* Kç ja K.P ne ovat ulottumattomia lukuja, toisin sanoen puhtaita lukuja, joissa yksikään ei liity mihinkään suuruuteen tai suuruuden väliseen suhteeseen.
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm

