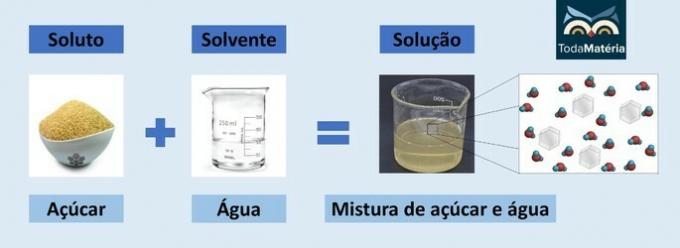
Liukoisuuskerroin (Cs) vastaa liuenneen aineen määrää, joka tarvitaan tietyn määrän liuottimen kyllästämiseen tietyissä lämpötila- ja paineolosuhteissa.
Jokaisella aineella on erilaiset liukoisuuskertoimet kullekin liuotintyypille.
Lämpötila voi myös vaikuttaa aineiden liukoisuuteen. Useimmille aineille lämpötilan nousu aiheuttaa myös lisääntyneen liukoisuuden kaasuja lukuun ottamatta.
Kaasuilla on erilaiset liukoisuuskertoimet paineen muuttuessa.
Esimerkki
Liukoisuuskerroin voidaan osoittaa kokeellisesti. Harkitse seuraavaa esimerkkiä:
Jos lisäät lusikallisen sokeria lasilliseen vettä, sokeri katoaa aluksi ja vedestä tulee makeaa.
Kuitenkin, jos lisää sokeria lisätään, tulee kohta, jossa se alkaa kerääntyä lasin pohjalle.
Siinä vaiheessa vesi saavutti liukoisuusrajansa. Mikä tahansa lisätty sokerin määrä kerääntyy pohjaan, kun liukoisuuskerroin on saavutettu.
tietää enemmän Liukoisuus.
Kuinka lasketaan liukoisuuskerroin?
Kaava liukoisuuskertoimen laskemiseksi on:
Cs = 100. m1 / m2
Missä:
Cs: liukoisuuskerroin
m1: liuenneen aineen massa
m2: liuottimen massa
lukea Liuotin ja liuotin.
Ratkaisujen luokitus
Liukoisuuskertoimen perusteella ratkaisut voidaan luokitella:
tyydyttymätön liuos
Liuosta pidetään tyydyttymättömänä, kun liuenneen aineen määrä on pienempi kuin Cs.
Tällöin liuotettavaan liuokseen voidaan lisätä vielä enemmän liuenneita aineita.
kyllästetty liuos
Liuos on kyllästetty, kun liuenneen aineen määrä on täsmälleen sama kuin Cs. Se on kyllästysraja.
Esimerkiksi NaCl: n liukoisuuskerroin on 36 g 100 g: aan vettä 20 ° C: n lämpötilassa.
Tämä tarkoittaa, että tämä määrä tekee liuoksesta tyydyttyneen. Jos 37 g NaCl: a lisätään 100 g: aan vettä dekantterilasissa, 1 g NaCl ei liukene ja kerääntyy dekantterilasin pohjaan.
Säiliön pohjalle jäänyttä liuosta kutsutaan sakaksi, pohjarungoksi tai lattiakappaleeksi.
Tätä ratkaisua kutsutaan nyt kyllästetty taustalla.
ylikyllästetty liuos
Ylikyllästetty liuos tapahtuu, kun liuenneen aineen määrä on suurempi kuin Cs.
Se on eräänlainen ratkaisu, jota on vaikea löytää ja melko epävakaa.
Tietää enemmän:
- liukoisuustuote
- Kemialliset ratkaisut
- Homogeeniset ja heterogeeniset seokset
- Liuosten laimennus
Harjoitus ratkaistu
Harkitse seuraavaa tilannetta:
Liukoisen aineen liukoisuuskerroin on 60 g / 100 g vettä (80 ° C). Kuinka määritetään 80 g veden kyllästämiseksi tarvittavan liuenneen aineen massa tässä lämpötilaolosuhteessa?
Tämän kysymyksen ratkaisemiseksi sinun on käytettävä seuraavaa kaavaa, koska liukoisuuskerroin on annettu.
Cs = 100. m1 / m2
Joten 80 g veden kyllästämiseksi tarvittavan liuoteainemassan löytämiseksi meillä on:
60 = 100. m1 / 80
m1 = 48 g
Harjoitukset
1. (PUC / SP - 2006) Tiedot:
BaSO: n liukoisuus = 1,0 x 10-5 mol. L-1
CaSO-liukoisuus = 5,0 x 10-3 mol. L-1
MgCO-liukoisuus = 1,0 x 10-3 mol. L-1
Mg: n (OH) liukoisuus = 5,0 x 10-4 mol. L-1
NaC: n liukoisuus = 6,5 mol. L-1
Suoritettiin neljä itsenäistä koketta sekoittamalla yhtä suuret määrät yhdisteiden vesiliuoksia alla ilmoitettuina pitoisuuksina.
Koe 1: BaCl2 (vesiliuos) 1,0x10-3 mol. L-1 ja Na2S04 (vesipitoinen) 1,0x10-3 mol. L-1
Koe 2: CaCl2 (vesiliuos) 6,0x10-3 mol. L-1 ja Na2S04 (vesipitoinen) 1,0x10-2 mol. L-1
Koe 3: MgCl2 (vesiliuos) 1,0x10-2 mol. L-1 ja Na2C03 (vesiliuos) 1,0x10-3 mol. L-1
Koe 4: MgCl2 (vesiliuos) 8,0x10-4 mol. L-1 ja NaOH (vesiliuos) 1,0x10-4 mol. L-1
Sakkaa muodostui:
a) vain kokeissa 1 ja 3.
b) vain kokeissa 2 ja 4.
c) vain kokeissa 1 ja 4.
d) vain kokeissa 1, 2 ja 3.
e) kaikissa kokeissa.
a) vain kokeissa 1 ja 3.
2. (UFRS) Mitkä ovat vesiliuokset, jotka sisältävät yhden liuenneen aineen, jolla voi olla tämän aineen taustakappale?
a) tyydyttyneitä ja ylikylläisiä.
b) vain tyydyttyneitä.
c) laimennettu tyydyttymätön.
d) vain ylikyllästetyt.
e) väkevöity tyydyttymätön.
b) vain tyydyttyneitä