Puhdas aine muodostuu yhden tyyppisistä kemiallisista lajeista, eli sen koostumus ja ominaisuudet ovat kiinteät. Sekoitus sisältää useampaa kuin yhtä komponenttityyppiä, joten sen organisaatio vaihtelee.
Siksi voimme erottaa puhtaan aineen seoksesta vasta kun tiedämme sen koostumuksen.
Kun verrataan lasillista vettä ja lasillista liuotettua sokeria, silmämme eivät huomaa mitään eroa. Kuitenkin, jos nautimme kahden lasin sisällön, huomaamme, että toinen on puhdasta ainetta ja toinen koostuu seoksesta.
puhtaita aineita
Puhdas aine on vain yhden kemiallisen lajin joukko, toisin sanoen sitä ei sekoiteta muihin.
Käytetään vettä esimerkkinä. Vesi (H2O) on tunnustettu ominaisuuksiltaan, ja tämän materiaalin erityisominaisuudet auttavat meitä tunnistamaan sen. Pää veden ominaisuudet he ovat:
| Tiheys | 1,00 g / cm3 |
|---|---|
| Fuusiopiste | 0 ° C |
| Kiehumispiste | 100 ° C |
Kun materiaalilla on kiinteät ja muuttumattomat ominaisuudet koko kokonaisuudessaan, sanomme sen olevan puhdas aine.
Kun laitamme pöytäsuolaa, natriumkloridia (NaCl) lasilliseen vettä ja sekoitamme, tapahtuu muutos.

Tuloksena on tuote, jonka veden ja suolan tiheys on välituote. Tämä johtuu siitä, että vesi ei ole enää puhdas aine ja siitä on tullut a Sekoita.
Kun yrität jäädyttää tätä seosta, huomaat, että sulamislämpötila on alle 0 ° C myös tämä seos ei kiehu 100 ° C: ssa, sen haihduttamiseksi tarvitaan enemmän lämpöä tuote.
Puhtaat yksinkertaiset ja yhdistetyt aineet
Puhtaat aineet luokitellaan yksinkertaisiksi, kun niiden koostumuksessa on vain yhden kemiallisen elementin atomeja.
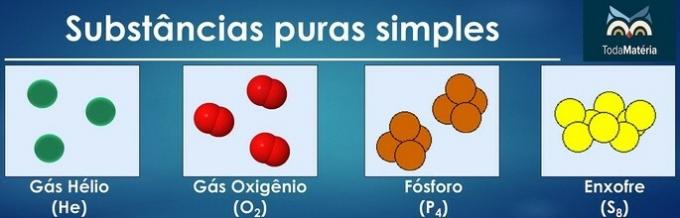
Kahden tai useamman kemiallisen elementin atomien järjestely muodostaa puhtaita komposiittiaineita.

Seokset
Seos vastaa kahden tai useamman puhtaan aineen yhdistämistä, joita kutsutaan komponenteiksi.
Toisin kuin puhtaat aineet, sen ominaisuudet eivät ole kiinteitä, koska ne riippuvat komponenttien osuudesta seoksessa.
Katso kuinka tiheys, fyysinen ominaisuus, vaihtelee veden kanssa sekoitetun suolan määrän mukaan.
| Suolan prosenttiosuus seoksen kokonaismassa |
Seoksen tiheys (g / cm3) 20 ° C: ssa |
|---|---|
| 1 | 1,005 |
| 8 | 1,056 |
| 12 | 1,086 |
| 16 | 1,116 |
| 26 | 1,197 |
Lähde: FURNISS, B. S. et ai. Vogelin käytännön orgaanisen kemian oppikirja. 4. toim. Lontoo: Longman, 1987. P. 1.312.
Siksi veden ja suolan lisäämisellä, missä tahansa suhteessa, on vaihteleva tiheys, joten emme voi luokitella seosta joko vedeksi tai suolaksi.
Homogeeniset ja heterogeeniset seokset
Homogeeniset seokset ovat sellaisia, jotka esittävät komponentit vain yhdessä faasissa ja siten samat ominaisuudet kaikissa pisteissä.

Kun havaitsemme visuaalisesti useampaa kuin yhtä faasia, seos luokitellaan heterogeeniseksi.

Yhteenveto puhtaista aineista ja seoksista
| Puhtaat aineet ja seokset | |
|---|---|
|
homogeeninen järjestelmä (vain yksi vaihe) |
puhdas aine (yksi komponentti) |
|
homogeeninen seos (useampi kuin yksi komponentti samassa vaiheessa) | |
|
heterogeeninen järjestelmä (useampi kuin yksi vaihe) |
puhdas aine (komponentti eri fysikaalisissa tiloissa) |
|
heterogeeninen seos (useampi kuin yksi komponentti useammassa kuin yhdessä vaiheessa) |
Jos haluat lisätietoja, tarkista nämä tekstit:
- Atomit
- Kemialliset alkuaineet
- Seosten erottaminen
Harjoitukset kommentoidulla palautteella
1. (UFMG) Näytteestä puhtaasta aineesta X määritettiin joitakin sen ominaisuuksia. Kaikilla vaihtoehdoilla on ominaisuuksia, joista on hyötyä aineen tunnistamisessa, paitsi:
a) tiheys.
b) näytemassa.
c) vesiliukoisuus.
d) kiehumislämpötila.
e) sulamislämpötila.
Väärä vaihtoehto: b) näytemassa.
a) OIKEA. Tiheys on aineen määrä tietyssä tilavuudessa. Materiaalikohtaisena ominaisuutena se on hyödyllinen aineen tunnistamiseksi.
b) VÄÄRIN. Massa on aineen määrä kehossa. Koska tätä ominaisuutta sovelletaan mihin tahansa aineeseen muodosta riippumatta, sitä ei voida käyttää aineen tunnistamiseen.
c) OIKEA. Liukoisuus on aineen kyky liueta tai ei tietyssä nesteessä. Materiaalikohtaisena ominaisuutena se on hyödyllinen aineen tunnistamiseksi.
d) OIKEA. Kiehumislämpötila vastaa nestemäisestä kaasumaiseen tilaan siirtymisen lämpötilaa. Materiaalikohtaisena ominaisuutena se on hyödyllinen aineen tunnistamiseksi.
e) OIKEA. Sulamislämpötila vastaa nestemäisestä kiinteään tilaan tapahtuvan muutoksen lämpötilaa. Materiaalikohtaisena ominaisuutena se on hyödyllinen aineen tunnistamiseksi.
2. (Vunesp) Kivennäisvesipullon etiketti on jäljempänä.
| Todennäköinen kemiallinen koostumus: |
|---|
| Kalsiumsulfaatti 0,0038 mg / l |
| Kalsiumbikarbonaatti 0,0167 mg / l |
Näiden tietojen perusteella voimme luokitella kivennäisveden seuraavasti:
a) puhdas aine.
b) yksinkertainen aine.
c) heterogeeninen seos.
d) homogeeninen seos.
e) kolloidinen suspensio.
Oikea vaihtoehto: d) homogeeninen seos.
a) VÄÄRIN. Vesi olisi puhdasta, jos sen koostumuksessa olisi vain H-molekyylejä2O.
b) VÄÄRIN. Yksinkertainen aine koostuu vain yhden kemiallisen elementin atomeista. Puhdas vesi ei myöskään ole yksinkertainen aine, koska sen muodostavat vety- ja happiatomit (H2O) se on luokiteltu komposiitti.
c) VÄÄRIN. Heterogeenisessä seoksessa on enemmän kuin yksi faasi, jolloin voimme tarkkailla vain vettä.
d) OIKEA. Koska sillä on vain yksi vaihe, järjestelmä on homogeeninen. Vesipulloa tarkasteltaessa voimme nähdä vain nesteen, koska kalsiumsulfaatti- ja kalsiumvetykarbonaattiyhdisteet liukenevat veteen ja ovat siten liuenneita.
e) VÄÄRIN. Kolloidisuspensio on heterogeeninen seos, jonka komponentit erotellaan mikroskoopilla.
3. (UCDB) Kemian laboratoriossa valmistettiin seuraavat seokset:
I. vesi / bensiini
II. vesi / suola
III. vesi / hiekka
IV. bensiini / suola
V. bensiini / hiekka
Mitkä näistä seoksista ovat homogeenisia?
a) Ei mitään.
b) Vain II.
c) II ja III.
d) I ja II.
e) II ja IV.
Oikea vaihtoehto: b) Vain II.
a) VÄÄRIN. Vesi on epäorgaaninen yhdiste ja bensiini orgaaninen yhdiste. Näillä aineilla ei ole kykyä olla vuorovaikutuksessa, ja koska niiden tiheys on erilainen, ne muodostavat heterogeenisen seoksen.
b) OIKEA. Suola, natriumkloridi, liukenee veteen muodostaen liuoksen, joka on homogeeninen seos.
c) VÄÄRIN. Hiekka, piidioksidi, muodostaa heterogeenisen seoksen veden kanssa.
d) VÄÄRIN. Suola on epäorgaaninen yhdiste ja bensiini orgaaninen yhdiste. Näillä aineilla ei ole kykyä olla vuorovaikutuksessa, ja koska niiden tiheys on erilainen, ne muodostavat heterogeenisen seoksen.
e) VÄÄRIN. Hiekka on epäorgaaninen yhdiste ja bensiini orgaaninen yhdiste. Näillä aineilla ei ole kykyä olla vuorovaikutuksessa ja ne muodostavat siten heterogeenisen seoksen.
4. (Ufes) Hyvin sekoitetussa järjestelmässä, joka koostuu hiekasta, suolasta, sokerista, vedestä ja bensiinistä, vaiheiden lukumäärä on:
a) 2.
b) 3.
c) 4.
d) 5.
e) 6.
Oikea vaihtoehto: b) 3.
VAIHE 1: Suola ja sokeri voivat olla vuorovaikutuksessa veden kanssa ja molekyylien välisten voimien kautta molekyylit sitoutuvat ja muodostavat liuoksen, joka on homogeeninen seos.
VAIHE 2: Vesi on epäorgaaninen yhdiste ja bensiini orgaaninen yhdiste. Näillä aineilla ei ole kykyä olla vuorovaikutuksessa, ja koska niiden tiheys on erilainen, ne muodostavat heterogeenisen seoksen.
VAIHE 3: Hiekka on silikaatti, jolla ei ole kemiallista affiniteettia veteen ja bensiiniin, joten se edustaa vaihetta.
5. (Mackenzie) Seos, jonka muodostavat:
a) jääkuutioita ja vesipitoista sokeriliuosta (glukoosi).
b) N kaasua2 ja CO2.
c) vesi ja asetoni.
d) vesi ja karviaismarjasiirappi.
e) kerosiini ja dieselöljy.
Oikea vaihtoehto: a) jääpalat ja sokeriliuos (glukoosi).
a) OIKEA. On mahdollista havaita kaksi vaihetta: jääkuutioita ja glukoosiliuosta, joten ne ovat heterogeeninen järjestelmä.
b) VÄÄRIN. Kaasut ovat aina homogeeninen seos.
c) VÄÄRIN. Vetysidoksia muodostuu propanonin karbonyylin ja vesimolekyylin välille. Koska ne ovat polaarisia aineita, asetoni kykenee liukenemaan veteen ja muodostamaan homogeenisen seoksen.
d) VÄÄRIN. Nämä kaksi komponenttia sekoittuvat muodostaen homogeenisen järjestelmän, koska karviaismarjasiirapista näemme vain punaisen nesteen, koska laimennus tapahtuu lisäämällä vettä.
e) VÄÄRIN. Molemmat ovat orgaanisia yhdisteitä ja kemiallisen affiniteetin vuoksi ne muodostavat yhden faasin, joka edustaa homogeenista järjestelmää.
Testaa tietosi harjoituksilla:
- Harjoitukset homogeenisille ja heterogeenisille seoksille
- Harjoitukset seosten erottamiseksi
- Harjoitukset aineen ominaisuuksista



