Nitraatit ovat epäorgaanisia yhdisteitä, jotka sisältävät anionia NO3-.
Typpi on perheestä 15, valenssikuoressa on 5 elektronia, ja sen on tehtävä kolme kovalenttista sidosta (jakamalla elektroneja) kahdeksan elektronia valenssikuoressa ja siten pysyä vakaa. Jokaisella hapella on kuitenkin 6 elektronia viimeisessä kuoressa, ja siksi kunkin sen atomin on muodostettava kaksi sidosta pysyäkseen vakaana.
Joten nitraattianionissa typpi on keskeinen elementti, joka muodostaa kaksoissidoksen yhden hapen kanssa, joka on stabiili, yksi sidos kahden muun hapen kanssa ja toinen kovalenttinen sidos datiivi. Tämä tarkoittaa, että yksi oksigeeneistä ei ole stabiili, sen on vastaanotettava vielä yksi elektroni, jolloin kokonaisvaraus on -1. Datiivin avulla typpi muodostaa sidoksen enemmän kuin se voisi tehdä, lahjoittamalla yhden elektronistaan, jolloin varaus on yhtä suuri kuin +1. Katso alla tämän anionin rakenne:
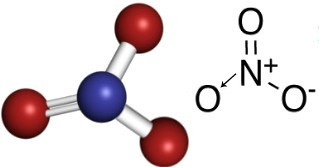
Tämä anioni voi vastaanottaa elektronin ja muodostaa sähköisesti neutraalin yhdisteen, epäorgaanisen suolan. Nämä yhdisteet ovat kaikki vesiliukoisia.
Nitraattien pääasialliset käyttökohteet ovat lääkkeet, kuten vasodilataattorit angina pectoriksen (kivun alhainen hapen saanti verenkierrosta sydänlihakseen) ja erektiohäiriöt Uros. Niitä käytetään myös lannoitteissa ja räjähteissä, kuten myöhemmin mainitaan.
Nitraatteja voidaan tuottaa typpihapon (HNO) neutralointireaktiolla.3) jossain määrin. Katso alla oleva esimerkki, jossa muodostui magnesiumnitraattia:
HNO3 + Mg (OH)2 → Mg (NO3)2+ H2O
Kolme pääesimerkkiä tämän tyyppisestä yhdisteestä ovat natriumnitraatti (NaNO3), kaliumnitraatti (KNO3) ja ammoniumnitraatti (NH4AT3). Kaikissa näissä tapauksissa kationit (Na+, K+ ja NH4+) antaa 1 elektroni nitraattianionille. Mutta todellisuudessa nämä vastakkaiset varaukset houkuttelevat toisiaan ja muodostavat tarkasti määritellyt ioniryhmät, jotka ovat kideverkkoa. Niinpä nitraatit ovat yleensä kiteisiä kiinteitä aineita, kuten alla on esitetty natriumnitraatin tapauksessa:
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
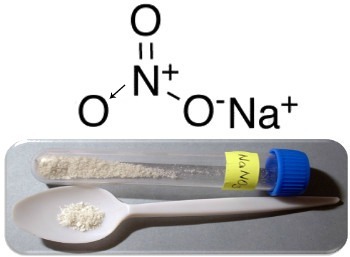
Tätä yhdistettä käytetään lannoitteiden valmistuksessa, mutta se tunnetaan pääasiassa nimellä Chilen suolakeittiö, koska Chilen aavikoilla on suuria saostumia. Se muuttuu kaliumnitraatiksi, jota käytetään eri aseissa ja räjähteissä käytettävän mustan jauheen valmistamiseen.

Sekä natriumnitraattia että kaliumnitraattia kutsutaan "saltpetreksi", jota käytetään laajalti nimellä säilykkeiden ja savustettujen lihojen värin säilöntäaineet sekä joissakin elintarvikkeissa suuremman tunteen antamiseksi kylläisyyttä. Niiden kulutus aiheuttaa kuitenkin vakavaa haittaa terveydelle, koska bakteerit voivat muuttaa näitä nitraatteja organismi nitriitteiksi ja myöhemmin nitrosamiineiksi, jotka ovat karsinogeenisia ja aiheuttavat pääasiassa syöpää vatsa. Nitriitit muuntavat myös veren hemoglobiinit, jolloin ne eivät kykene kuljettamaan happea.
Nitraattien liiallisen saannin tärkeimmät syyt ovat typpilannoitteiden käyttö vihannesten viljelyssä.
Saltpeter on myös vaarallinen, koska se lisää natriumionien pitoisuutta kehossa, mikä voi aiheuttaa sydänongelmia, kuten korkea verenpaine.
O ammoniumnitraatti sitä käytetään myös lannoitteena ja räjähteinä, ja sitä käytettiin jopa polttoöljyn kanssa 11. syyskuuta 2001 tehdyssä terrori-iskussa World Trade Center -rakennuksiin.

Hyökkäys Maailman kauppakeskukseen käytti ammoniumnitraattia *
* Kuvan tekijänoikeudet: Dan Howell ja Shutterstock.com
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Nitraatit"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/nitratos.htm. Pääsy 27. kesäkuuta 2021.
Kemia

Jokapäiväiset suolat, kalsiumkarbonaatti, natriumkloridi, natriumfluoridi, kaliumnitraatti, natriumnitraatti natrium, natriumkarbonaatti, natriumbikarbonaatti, natriumbikarbonaatti, natriumsulfiitti, suolapitoinen sooda.


