Isotermilises muundumises mahu ja rõhu kõikumine teatud gaasi, kuid püsiv temperatuur; siit ka isotermilise nime (kreeka keeles: iso = võrdne; termo = kuumus).
Teadlased Boyle ja Mariotte viisid eraldi läbi sarnased katsed ja saadud tulemus oli: rõhu suurenedes gaasi maht väheneb.
Mõelge vaid näiteks süstla kolbile. Kui rakendame sellele kolvile välist survet, see tähendab, et rõhu suurendamisel väheneb süstla hõivatud õhu maht ja vastupidi.
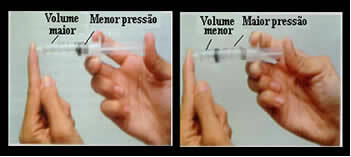
Maht ja rõhk on pöördvõrdelised: vasakpoolsel paneelil on rõhk väike ja õhu poolt hõivatud maht suur. Paremal, kui süstlakolbile avaldatakse suuremat survet, väheneb maht.
See pole üksikjuhtum, see on midagi, mida korratakse gaaside puhul ühise korrapärasusega. Seetõttu öeldi see asjaolu seaduse kujul, mida saab kirjeldada järgmiselt:
| Boyle'i seadus või Boyle-Mariotte'i seadus: Konstantse temperatuuri korral on gaasi kindla massiga hõivatud maht pöördvõrdeline selle rõhuga. |
See tähendab, et kui me gaasi rõhu kahekordistame, väheneb selle maht poole võrra ja nii edasi. Kui kaks sellist kogust on pöördvõrdelised, on nende korrutis konstant; seega saab matemaatiliselt seda suhet kujutada järgmiselt:
| P.V = k |
Kus k = konstant.
Seega, kui esimeses olukorras on teatud gaasi rõhuväärtus P1 ja selle vastav maht V1, siis peame:
| P1. V1 = k |
Kui suurendame seda rõhku väärtusele P2, muudetakse ka selle maht väärtuseks V2 ja jälle peame:
| P2 . V2 = k |
Seega jõuame järeldusele:
| P1. V1 = P2. V2 |
Seda püsivust saab näha allolevas tabelis toodud näite abil fikseeritud massiga gaasi rõhkude ja mahtude kohta:
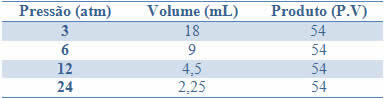
Nende väärtuste graafiku koostamisel näeme kõvera moodustumist.
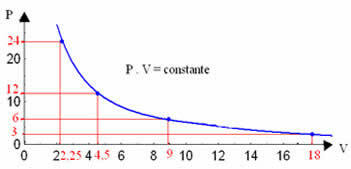
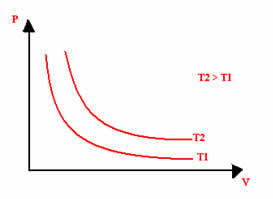
Isotermilise muundamise graafiline esitus on alati hüperbool, olenemata rõhu, mahu ja temperatuuri väärtustest, mille juures katse läbi viidi. Seda hüperbooli nimetatakse isoterm; nii et nagu allpool olevalt graafikult näha võib, põhjustavad erinevad temperatuurid erinevaid isoterme.
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/quimica/transformacao-isotermica-ou-lei-boyle.htm

