A termodünaamika teine seadus määrab, millised tingimused selleks kehtivad soojust ümber töötamiseks soojusmasinates ja külmikutes. See käsitleb ka määratlust entroopia kui nähtus, mis on võimeline mõõtma osakeste disorganiseerumist füüsilistes süsteemides.
Loe ka: Kalorimeetria – füüsika haru, mis uurib soojusvahetust
Kokkuvõte termodünaamika teisest seadusest
Termodünaamika teist seadust esindavad Clausiuse ja Kelvin-Plancki väited.
Clausiuse väide käsitleb soojuse liikumist kuumemast kehast külmemasse kehasse.
Kelvin-Plancki avaldus käsitleb termiliste seadmete võimetust kogu oma soojust muundada tööd.
Termodünaamika teist seadust rakendatakse soojusmasinatele ja külmikutele.
Carnot' tsükkel on soojusmasinate maksimaalne efektiivsustsükkel.
Carnot' tsüklil on neli etappi: pöörduv isotermiline paisumine, pöörduv adiabaatiline paisumine, pöörduv isotermiline kokkusurumine ja pöörduv adiabaatiline kokkusurumine.
Carnot' teoreem viitab saagisele Carnot masinad.
Mis on termodünaamika teine seadus?
Termodünaamika teine seadus on a Seadus, mis käsitleb termodünaamilistes protsessides esinevaid piiranguid. Seda kuulutasid välja füüsikud Rudolf Clausius (1822-1888), Lord Kelvin (1824-1907) ja Max Planck (1858-1947), nagu näeme allpool:
Füüsik ja matemaatik Rudolf Clausius väitis, et soojuse juhtivusvool toimub kõrgema temperatuuriga kehast madalama temperatuuriga kehasse. madalam temperatuur, seetõttu ei ole pöördprotsessi toimumine loomulik, seetõttu on vaja seda tööd teha süsteem. Sellega teatas ta:
Võimatu on läbi viia protsessi, mille ainsaks toimeks on soojuse ülekandmine külmemalt kehalt kuumemale.|1|
Matemaatiline füüsik William Thomson, tuntud kui Lord Kelvin, koos füüsik Max Plancki kaastööga, väitis 100% efektiivsusega termoseadmete võimatust, kuna soojuskadu on alati olemas.
Termodünaamika teise seaduse rakendused
Termodünaamika teist seadust rakendatakse soojusmasinatele ja külmikutele.
Masinate termodünaamika teine seadus soojus
Et Soojusmasinad on võimelised soojust tööks muutma. Kuum allikas varustab soojust soojusmasinaga, mis muudab selle tööks. Ülejäänud soojuse saadab see külmaallikasse, nagu on kujutatud alloleval pildil:
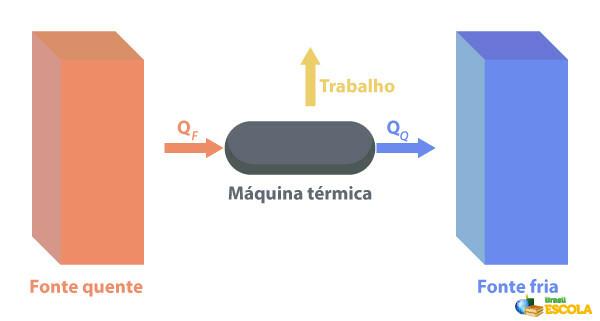
Mõned soojusmasinate näited on: auru- ja petrooleumiturbiinid reaktiivlennukites, sisepõlemismootorid, termotuumareaktorid.
Termodünaamika teine seadus külmikutes
Külmikud on masinad, mis Need töötavad mootorite soojendamisele vastupidiselt., kus nad eemaldavad soojust piirkonnast, millel on temperatuuri madalamal temperatuuril ja tarnige see kõrgema temperatuuriga piirkonda. Kuna see pole loomulik, peab masin tegema elektrienergiat kasutavaid töid, nagu on kirjeldatud alloleval pildil:
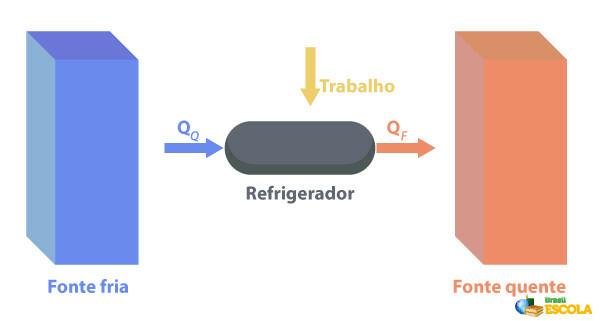
Mõned külmikute näited on külmikud ja kliimaseadmed.
Entroopia ja termodünaamika teine seadus
A Termodünaamika teine seadus viitab entroopia olemasolule, üks füüsiline kogus vastutab füüsikalises süsteemis olevate osakeste desorganiseerumise astme või süsteemi pöördumatuse määra mõõtmise eest. Soojusmasinatega seotud termodünaamilised protsessid, mis on spontaanne, vältimatu, pöördumatu ja ekspansiivne. Sellega on võimalik vaid jälgida ja ohjeldada protsesside volatiilsuse astet. Entroopia suurenedes suureneb ka süsteemi korratuse määr.
A Entroopia nomenklatuur on kreeka päritolu ja tähendab "muutust"., "muuda", seega kasutatakse seda Füüsiline juhuse ja korratuse näitamiseks. Entroopiat saab arvutada järgmise valemi abil:
\(∆S=\frac{∆U}T\)
\(∆S\) on entroopia muutus, mõõdetuna [J/K].
\(∆U\) on siseenergia muutus, mõõdetuna džaulides [J].
T on temperatuur, mõõdetuna kelvinites [K].
Statistilisest vaatenurgast arvutatakse entroopia järgmise valemiga:
\(S=k\cdot ln\ Ω\)
S on entroopia, mõõdetuna [J/K].
k on Boltzmanni konstant, see on väärt \(1,4\cdot 10^{-23}\ J/K\).
Ω on süsteemi võimalike mikroolekute arv.
Loe ka: Soojuse leviku protsessid
Termodünaamika teise seaduse valemid
Soojusmasinad ja külmikud
\(Q_Q=W+Q_F\)
\(Q_Q\) on kuuma allika soojus, mõõdetuna džaulides [J].
W on soojusmasina tehtud töö, mõõdetuna džaulides [J].
\(Q_F\) on külmaallika soojus, mõõdetuna džaulides [J].
Seda saab esindada:
\(W=Q_Q-Q_F\)
W on soojusmasina tehtud töö, mõõdetuna džaulides [J].
\(Q_Q\) on kuuma allika soojus, mõõdetuna džaulides [J].
\(Q_F\) on külmaallika soojus, mõõdetuna džaulides [J].
Külmikud
\(η=\frac{Q_F}{Q_Q-Q_F}\)
\(η\) on külmiku efektiivsus.
\(Q_F\) on külmaallika soojus, mõõdetuna džaulides [J].
\(Q_Q\) on kuuma allika soojus, mõõdetuna džaulides [J].
Seda saab kujutada järgmiselt:
\(η=\frac{Q_F}W\)
\(η\) on külmiku efektiivsus.
\(Q_F\) on külmaallika soojus, mõõdetuna džaulides [J].
W on soojusmasina tehtud töö, mõõdetuna džaulides [J].
Näited valemite rakendamisest
Näide 1: Arvutage töö, mida soojusmasin teeb tsükli jooksul, mis võtab kuumalt allikalt vastu 500 J soojust ja edastab külmale allikale ainult 400 J soojust.
Soojusmasina töö arvutamiseks kasutame valemit:
\(W=Q_Q-Q_F\)
Avalduses märgitud väärtuste asendamine:
\(W=500–400\)
\(W=100\J\)
Soojusmasina töö oli 100 džauli.
Näide 2: Milline on külmiku kasutegur, mis võtab kuumalt allikalt vastu 150 J soojust ja edastab 50 J soojust külma allikale?
Külmiku efektiivsuse arvutamiseks kasutame valemit:
\(η=\frac{Q_F}{Q_Q-Q_F}\)
Asendades avalduses antud väärtused, saame:
\(η=\frac{50}{150-50}\)
\(η=\frac{50}{100}\)
\(η=0,5\)
Saagise korrutamine 100% -ga:
\(η=0,5\cdot100%\)
\(η=50\%\)
Külmiku kasutegur on 50%.
Carnot' tsükkel
Carnot' tsükkel oli välja töötanud teadlane Sadi Carnot (1796-1832), mille eesmärk on tuvastada maksimaalne kasutegur, mille võib saavutada kuuma ja külma allika vahel töötava soojusmootoriga.
Oma uuringute põhjal tuvastas Carnot, et soojusmasina maksimaalse efektiivsuse saavutamiseks on see nii vajalik, et tema protsess oleks pöörduv, seetõttu töötas ta välja maksimaalse saagikuse tsükli, mida nimetatakse tsükliks Carnot ja Selle kaudu töötavat soojusmasinat nimetatakse Carnot' soojusmootoriks.. Kuna Carnot' tsükkel on pöörduv, saab seda ümber pöörata, nii töötati välja külmikud.
Carnot' tsükkel, olenemata kasutatavast ainest, koosneb neljast protsessist, mida on kirjeldatud rõhu ruumala (p × V) graafikul, nagu näeme alloleval pildil:
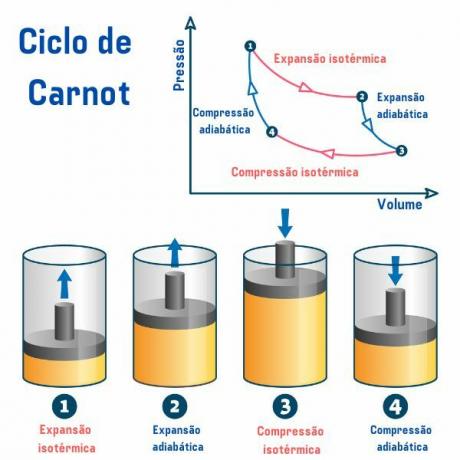
1. protsess, punktist 1 → 2: toimub pöörduv isotermiline paisumine (protsess, mille käigus temperatuur jääb konstantseks), mille käigus gaas (või süsteem) töötab ja omandab kuumast allikast teatud koguse soojust.
2. protsess, punktist 2 → 3: toimub adiabaatiline paisumine (protsess, mille käigus toimub soojusvahetus väliskeskkonnaga) pöörduv, mille puhul soojusvahetust ei toimu soojust soojusallikatega, kuid gaas töötab ja selle siseenergia väheneb, mis põhjustab gaas vähenemise temperatuuri.
3. protsess, punktist 3 → 4: toimub pöörduv isotermiline kokkusurumine, mille käigus gaas saab tööd ja annab külmaallikale teatud koguse soojust.
4. protsess, punktist 4 → 1: toimub pöörduv adibaatiline kokkusurumine, mille korral soojusvahetust soojusallikatega ei toimu ja gaas on kuumutatakse, kuni see saavutab kuuma allika temperatuuri, ja asetatakse sellega kokkupuutesse, lõpetades selle tsükkel.
termodünaamika seadused
Termodünaamika seadused on neli seadust, mis juhivad kogu uurimist termodünaamika, uurige ruumala, temperatuuri ja rõhu ning muude füüsikaliste suuruste, näiteks soojuse ja energia vahelisi seoseid.
Termodünaamika nullseadus: on seadus termiline tasakaal, uurib see soojusvahetust erineva temperatuuriga kehade vahel.
termodünaamika esimene seadus: on termodünaamiliste süsteemide energia jäävuse seadus, mis uurib soojuse muundumist tööks ja/või siseenergiaks.
Termodünaamika teine seadus: see on seadus, mis käsitleb soojusmasinaid, külmikuid ja entroopiat.
Termodünaamika kolmas seadus: on seadus absoluutne null, uurib ta selle temperatuuri mõju.
Loe ka: Soojusmasinate jõudlus
Lahendas ülesandeid termodünaamika teise seaduse kohta
küsimus 1 Määrake Carnot' mootori kuumaallika temperatuur, teades, et külma allika temperatuur on 450 K ja selle kasutegur on 80%.
a) 2250 K
b) 450 000
c) 1500 tuhat
d) 900 000
e) 3640 K
Resolutsioon:
Alternatiiv A. Kuuma allika temperatuuri arvutame Carnot' mootori efektiivsuse valemi alusel:
\(η=1-\frac{T_F}{T_Q} \)
\(80 \%=1-\frac{450}{T_Q} \)
\(\frac{80}{100}=1–\frac{450}{T_Q} \)
\(0,8=1-\frac{450}{T_Q} \)
\(0,8-1=-\frac{450}{T_Q} \)
\(-0,2=-\frac{450}{T_Q} \)
\(0,2=\frac{450}{T_Q} \)
\(T_Q=\frac{450}{0,2}\)
\(T_Q=2250\ K\)
küsimus 2 (Cefet-PR) Termodünaamika 2. printsiibi võib öelda järgmiselt: “Masinat on võimatu ehitada tsüklitena töötav soojusenergia, mille ainsaks toimeks on soojuse eemaldamine allikast ja selle integreerimine muundamiseks töö". Laiendusena viib see põhimõte meid järeldusele, et:
a) Alati on võimalik ehitada termomasinaid, mille kasutegur on 100%.
b) iga soojusmasin vajab ainult ühte soojusallikat.
c) soojus ja töö ei ole homogeensed suurused.
d) iga soojusmasin ammutab soojust kuumast allikast ja suunab osa sellest soojusest külma allikasse.
e) ainult külma allikaga, mille temperatuur on alati 0 °C, oleks teatud soojusmasinal võimalik soojust täielikult tööks muuta.
Resolutsioon:
Alternatiiv D. See põhimõte annab meile teada, et kuumast allikast kogu soojust on võimatu eemaldada ja külma allikasse üle kanda.
Märge
|1| Füüsika põhikursus: vedelikud, võnkumised ja lained, soojus (vol. 2).
Autor: Pamella Raphaella Melo
Füüsika õpetaja
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/fisica/segunda-lei-da-termodinamica.htm

