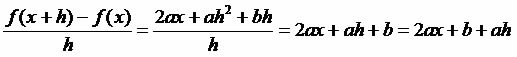A sublimatsioon See on aine füüsikalise oleku muutus, mida iseloomustab otsene üleminek tahkest faasist gaasifaasi, ilma vedelat faasi läbimata. Rangelt võttes võib sublimeerida iga aine, kuid teatud rõhu ja temperatuuri tingimustes. Sublimatsioon on korrelatsioonis tahke faasi aururõhuga, aga ka tahkete ainete molekulidevaheliste interaktsioonidega.
Seda protsessi saab kergesti jälgida kuivjää tükis, mis koosneb tahkest süsinikdioksiidist. Süsinikdioksiid sublimeerub rõhu all ja toatemperatuuril. Sublimatsioonile vastupidist protsessi võib nimetada resublimatsiooniks või ladestumiseks. Sublimatsiooni toimumiseks peab aine energiat neelama, seega peetakse seda endotermiliseks protsessiks.
Loe ka: Millised on aine füüsikalised olekud?
Kokkuvõte sublimatsioonist
Sublimatsioon on otsene üleminek tahkest faasist gaasifaasi, läbimata vedelat faasi.
Aine sublimatsiooni jälgimiseks on vajalikud kindlad rõhu ja temperatuuri tingimused.
Sublimatsiooni mõjutavad termodünaamilised aspektid, nagu aururõhk tahkes faasis ja molekulidevahelised interaktsioonid.
Sublimatsioon on endotermiline protsess.
Sublimatsiooni näide on see, mis toimub kuivas jääs, mis koosneb tahkest süsinikdioksiidist.
Mis on sublimatsioon?
sublimatsioon on otsene üleminek tahkest faasist gaasifaasi, läbimata vedelat faasi. Mõne tahke aine puhul esineb see teatud temperatuuri ja rõhu tingimustes. See üleminek on oleku muutumise füüsiline protsess, mis ei hõlma keemilisi reaktsioone.
Pöördprotsessi, st otsest üleminekut gaasilisest faasist tahkesse faasi nimetatakse erinevalt. Mõned autorid kasutavad selle faasimuutuse jaoks sõna sublimatsioon, teised aga kasutavad "resublimatsiooni" ja isegi "sadestumist".
Kuidas sublimatsioon töötab
Sublimatsiooni ja aurustumise vahele võib tõmmata paralleeli. Mõlemal juhul on lõpp-punkt gaasifaas. Erinevus on ilmselgelt algfaasis: tahke aine sublimeerimiseks ja vedelik aurustamiseks.
Mõlemal juhul on surve mõju devapor ja ka termodünaamilised aspektid, mis hõlmavad soojust ja molekulidevahelisi interaktsioone.
Mis on aururõhk?
Vedelikku sisaldavas suletud anumas on võimalik tajuda, et vedelfaasi ja aurufaasi vahel on tasakaal. Selle põhjuseks on asjaolu, et isegi allpool keemistemperatuuri on olemasolev energia piisav, et mõned vedeliku molekulid eralduksid ja aurudesse läheksid. Mõned aurumolekulid võivad aga ka uuesti kondenseeruda ja naasta vedelasse faasi, mis näitab protsessi pöörduvust.
See aur on valmistatud aine (on mass ja maht), harjutused surve vedeliku pinnale, tuntud kui aururõhk. See ei sõltu mitte vedeliku kogusest, vaid temperatuurist, sest mida kõrgem on temperatuur, seda kergemini eralduvad molekulid vedelast faasist.
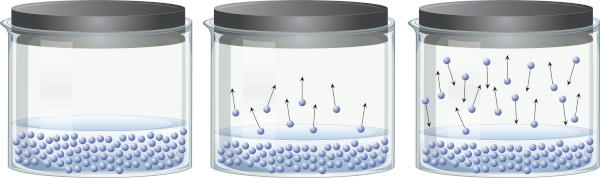
Vedelikke, millel on tavatemperatuuril kõrge aururõhk, nimetatakse lenduvateks. Näiteks 25°C juures on etüüleetri aururõhk 0,58 atm, atsetooni (propanooni) aururõhk on 0,29 atm, vee aururõhk aga 0,023 atm. Muide, kui aururõhk on identne atmosfäärirõhuga, siis vedelik keeb. Aururõhu kohta lisateabe saamiseks klõpsake nuppu siin.
Aururõhk ja sublimatsioon
Kuigi vähemal määral, tahketel ainetel on ka aururõhk, kuid palju madalam kui vedelike oma. Näiteks isegi temperatuuril 1000 K on raua aururõhk vaid 9,21 x 10-20 atm. Mõned tahked ained, näiteks jood, suudavad siiski sublimeerida, tekitades tavatemperatuuril kõrgemat aururõhku (4 x 10-4 atm).
See on võimalik ainult siis, kui molekulid lähevad tahkest olekust otse gaasilisse olekusse. Et see juhtuks, tahke aine molekulid peavad esinema molekulidevahelised interaktsioonid nõrk (näiteks joodis on need indutseeritud dipool-indutseeritud dipooli tüüpi).
Samuti on näha, et sublimatsiooniprotsess on endotermiline, see tähendab, et tahke aine molekulid peavad absorbeerima energiat soojuse kujul, et nad saaksid katkestada molekulidevahelised interaktsioonid ja minna auru olekusse. Kaasatud soojushulka saab mõõta termodünaamilise suuruse abil, mida nimetatakse sublimatsiooni entalpiaks.
Faaside diagramm
To teada, millises rõhu- ja temperatuurivahemikus tahke aine sublimatsioon toimub, peate oma faasidiagrammi hindama. Vaatame süsinikdioksiidi, CO juhtumit2.

Faasidiagrammil koondavad olekute (tahke, vedel ja gaasiline) vahelised piirijooned rõhu ja temperatuuri väärtused toimub oleku muutus. CO2 juhtumit jälgides on märgata, et 1 atmosfääri rõhul läheb tahke faas otse aurufaasi temperatuuril -78,5 °C, mis iseloomustab sublimatsiooni.
Süsinikdioksiidil on vedel faas ainult rõhul üle 5,11 atmosfääri ja sellest rõhust kõrgemal pole sublimatsioon enam võimalik. Faasidiagrammi kohta lisateabe saamiseks klõpsake nuppu siin.
näiteid sublimatsioonist
Kuiv jää: kuivjää, mida sageli kasutatakse pidudel ja üritustel uduefektide tegemiseks, on tegelikult tahkes olekus süsinikdioksiid.

koipallid: koipallid on valmistatud naftaleenist, aromaatsetest orgaanilistest ühenditest. Seda kasutatakse halva lõhna eemaldamiseks ja ka ööliblikate, prussakate ja muude mürgiste loomade peletamiseks, mistõttu on tavaline, et neid kasutatakse kappides või isegi pissuaarides.

Kampar: Iseloomuliku lõhnaga kamperkivikesed võivad samuti sublimeerida. Need aitavad ka sääski eemale peletada ja hallitust ära hoida.

Jood: halogeenide hulka kuuluv mittemetall läbib samuti sublimatsiooni.

Esitatud ainete hulgas on aga ainult süsinikdioksiid läbib ümbritseva keskkonna tingimustes sublimatsiooni. Teised võivad isegi sublimatsiooni korral läbida normaalse sulandumise rõhu all, milles me elame.
Loe ka: Plasma – aine neljas olek
Lahendati harjutusi sublimatsiooni kohta
küsimus 1
(Fuvest 2020) Supermarketites on tavaline leida nn külmkuivatatud toiduaineid, nagu puuvilju, köögivilju ja liha. Külmkuivatatud toidud sobivad tarbimiseks ka pärast pikka aega, isegi ilma külmkapita. Mõiste "lüofiliseeritud" nendes toiduainetes viitab külmutamisprotsessile ja sellele järgnevale dehüdratsioonile vee sublimatsiooni teel. Vee sublimatsiooni toimumiseks on vaja tingimuste kombinatsiooni, nagu on näidatud rõhu-temperatuuri graafikul, kus jooned tähistavad faasisiirdeid.
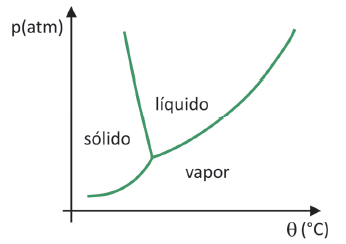
Hoolimata sellest, et tegemist on protsessiga, mis nõuab tööstuslikult teatud tehnoloogia kasutamist, on tõendeid selle kohta, et inimesed Andide kõrgeimates piirkondades elanud eelkolumbuslased suutsid toitu külmkuivatada, võimaldades seda säilitada rohkem aega. Kontrollige alternatiivi, mis selgitab loomuliku külmkuivatamise protsessi:
a) Vee sublimatsioon toimus mägedes madalate temperatuuride ja kõrge atmosfäärirõhu tõttu.
b) Toit viidi pärast looduslikku külmutamist külmadel perioodidel mägede madalaimasse ossa, kus atmosfäärirõhk oli madalam, mis tegi sublimatsiooni võimalikuks.
c) Temperatuuri tõstmiseks pandi toitu päikese kätte ja madal kohalik atmosfäärirõhk soodustas tahkumist.
d) Temperatuurid olid külmadel perioodidel piisavalt madalad, et toiduaineid külmutada, ja madal atmosfäärirõhk kõrgmägedes võimaldas sublimatsiooni.
e) Pärast loomulikku külmutamist pressiti toiduaineid rõhu suurendamiseks, et saaks toimuda sublimatsioon.
Vastus: D-täht.
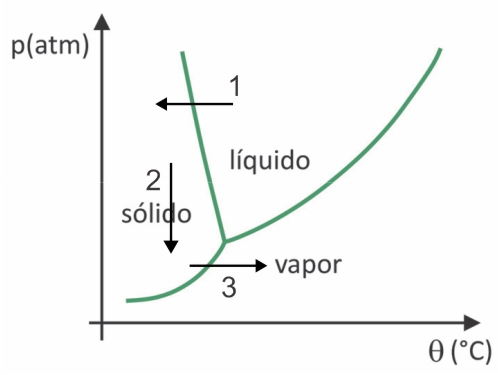
Lüofiliseerimisel toimub vee külmutamine koos järgneva sublimatsiooniga. Kolumbuse-eelsed rahvad võisid sellist protsessi läbi viia, kuna talvel võib vesi külmuda (nool 1) ja Andide kõrgeimate piirkondade madala rõhuga (nool 2) võib see sublimeeruda (nool 3).
küsimus 2
(Uerj 2005) Jahutusprotsessides laialdaselt kasutatav kuiv jää ehk tahkunud süsinikdioksiid läbib ümbritseva keskkonna tingimustes sublimatsiooni. Selle transformatsiooni käigus ilmnevad muuhulgas energia varieerumise ja interaktsioonide katkemise nähtused.
Need nähtused liigitatakse vastavalt järgmiselt:
a) eksotermiline – interioonne
b) eksotermiline – tuumadevaheline
c) isotermiline – interatomiline
d) endotermiline – molekulidevaheline
Vastus: D-täht.
Sublimatsioon on endotermiline protsess, kuna see nõuab soojuse neeldumist, et katkestada interaktsioonid, mis hoiavad tahke faasi molekule kompaktsena. Need interaktsioonid on molekulidevahelist tüüpi.
Autor Stefano Araujo Novais
Keemia õpetaja