THE ühine kontsentratsioon, mida nimetatakse ka kontsentratsiooniks g/l, on lahustunud aine massi suhe lahuse ruumalas.
Matemaatiliselt väljendatakse ühist kontsentratsiooni järgmise valemiga:
C = m/v
kus,
C: tavaline kontsentratsioon;
m: lahustunud aine mass;
V: lahuse maht.
Kõige sagedamini kasutatav ühik ühiseks kontsentratsiooniks on g/l, kuna lahustunud aine mass arvutatakse grammides (g) ja lahuse maht liitrites (L).
Näiteks merevees on palju lahustunud sooli ja naatriumkloriid (NaCl), rahvasuus tuntud ka lauasoolana, on üks neist.
Naatriumkloriidi kontsentratsioon merevees on keskmiselt 2,5 g/l. Niisiis, igas 1 liitris merevees, mis on lahus, on 2,5 grammi soola, mis on lahustunud aine.
Kuidas arvutada ühist kontsentratsiooni?
Lahus on homogeenne segu, mis moodustub suuremas koguses lahustis lahustunud ainest, mida nimetatakse lahustunud aineks.
Seega viitab tavaline kontsentratsioon lahustunud aine kogusele antud lahuse mahus. Mida rohkem lahustunud ainet lahuses on, seda kontsentreeritum see on. Vastasel juhul, st madal lahustunud aine näitab, et lahus on lahjendatud.
Näide 1: Mis on 2,6 g hõbejodiidi (AgI) lahuse kontsentratsioon g/l 1 liitris lahuses?
Kui on antud lahustunud aine kogus ja lahuse maht, ühendame väärtused lihtsalt ühisesse kontsentratsiooni valemisse, et leida selle väärtus.
Seetõttu on hõbejodiidi 2,6 g/l lahuses 2,6 g lahustunud ainet igas 1 liitris lahuses.
Näide 2: Kui suur on lahusti aurustamine 500 ml soolalahusest kontsentratsiooniga 6 g/l, milline on saadud lahustunud aine mass?
Pange tähele, et mõnes arvutuses leiame kirjeldatud ühise kontsentratsiooni, et saaksime arvutada lahustunud aine massi.
Samuti on vaja pöörata tähelepanu ühikutele. Kuna tavaline kontsentratsioon on antud g/l, siis sel juhul peame enne valemi rakendamist teisendama ruumalaühiku.
Kuna 1 l sisaldab 1000 ml, vastab 500 ml 0,5 liitrile.
Seega saadi lahusti aurustamisel lahusest kontsentratsiooniga 6 g/l 12 g lahustunud ainet.
Hankige sisuga rohkem teadmisi:
- Lahuse kontsentratsioon
- molaarne kontsentratsioon
- Lahuste lahjendamine
Lahendati ühiseid keskendumisharjutusi
Varem omandatud teadmiste kontrollimiseks kasutage järgmisi küsimusi.
küsimus 1
(Unicamp) Lahusti aurustatakse täielikult 250 ml MgCl vesilahusest2 kontsentratsiooniga 8,0 g/l. Mitu grammi lahustunud ainet saadakse?
a) 8.0
b) 6.0
c) 4.0
d) 2.0
e) 1,0
Õige alternatiiv: d) 2.0.
küsimus 2
Vaata allolevat pilti.
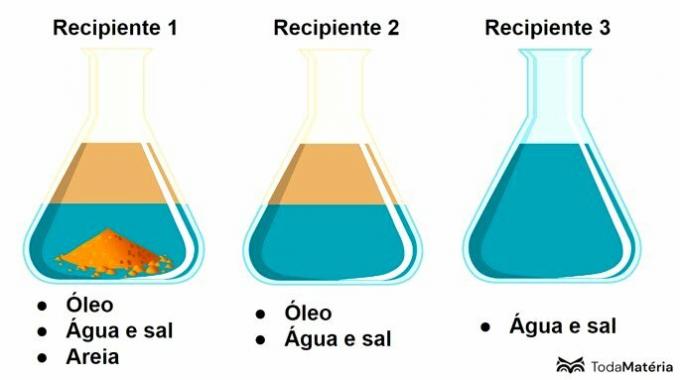
Selles skeemis sisaldab konteiner 3 a
a) heterogeenne segu
b) puhas aine
c) Lahendus
d) kolloidsegu
Õige alternatiiv: c) Lahendus.
Mahuti 3 sisaldab lahust, mis on lahustunud ainest ja lahustist moodustunud homogeenne segu, kus lahustunud aineks on sool ja lahustiks vesi.
Üldiselt võib öelda, et lahustunud aine on komponenti kõige väiksemas koguses ja lahustit esineb suurimas koguses.
Mahuti 1 kujutab endast 3 faasi heterogeenset segu ja konteiner 2 vastab 2 faasi heterogeensele segule.
küsimus 3
Lahus valmistati 4,0 g magneesiumkloriidi MgCl lahustamisega2 kuni saavutatakse kontsentratsioon 2,0 g/l. Kui suur maht lahust valmistati?
a) 1 l
b) 2 liitrit
c) 4 liitrit
d) 6 liitrit
Õige alternatiiv: b) 2 L.
Vaadake rohkem kommenteeritud lahendusega probleeme aadressil tavalised keskendumisharjutused.
Bibliograafilised viited
FONSECA, M. R. M. keemia, 1. 1. toim. São Paulo: Atika, 2013.
SANTOS, W.L.P; MOL, G.S. Kodaniku keemia, 1. 2. toim. São Paulo: toimetaja AJS, 2013.
USBERCO, J. Ühendage keemia, 1. 2. toim. São Paulo: Saraiva, 2014.
- Ühise keskendumise harjutused koos kommenteeritud tagasisidega
- keemilised lahused
- Lahusti ja lahusti: mis need on, erinevused ja näited
- Lahuse kontsentratsioon
- Lahustuvus
- Molaarsus või molaarne kontsentratsioon: mis see on, valem ja kuidas arvutada
- Lahuste lahjendamine
- Harjutused aine omaduste kohta