sooritada arvutamine entalpia reaktsioonist see tähendab energiamuutuste määramist, mis tekkis alates reagentide segunemisest kuni toodete moodustumiseni. Allolevas võrrandis on reaktiivide ja toodete esitus
A + B → C + D
A + B = reaktiivid
C + D = Tooted
Igal reaktsioonis osalejal on entalpia (H), see tähendab, et igal osalejal on teatud hulk energiat. Reaktsiooni käigus katkevad sidemed reagentide vahel ja tekivad sidemed toodete aatomite vahel. Sel viisil luuakse keemilise reaktsiooni käigus energia varieeruvus.
Reaktsiooni entalpia arvutamiseks on kõigepealt vaja teada iga osaleja individuaalset entalpiat. Tavaliselt annavad harjutused alati reagentide ja toodete entalpia väärtused. Näiteks:
ZnS+O2 → ZnO + SO2
HZnS = -49,23 Kcal/mol
HO2 = 0 Kcal/mol
HZnO = -83,24 Kcal/mol
HSO2 = -70,994 Kcal/mol
Kui meil oleks lihtaine, oleks entalpia väärtus null. Siiski on tähelepanuväärne, et kui lihtaine on reaktsioonis allotroop, peame olema ettevaatlikud, et teada saada, kas tegemist on seda ainet moodustava keemilise elemendi kõige stabiilsema allotroopiga. O
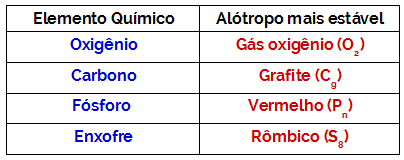
allotroop stabiilsema entalpia on alati null, nii et harjutus ei täida seda näidust. Vaadake tabelit elementidega, mis moodustavad allotroope ja mis on stabiilsemad:
MÄRKUS: Elemendi kõige stabiilsem allotroopne vorm näitab ainet, mida leidub looduses suuremas koguses.
Reaktsiooni entalpia arvutamist nimetatakse tavaliselt entalpia variatsiooniks ja seda tähistatakse alati akronüümiga ∆H. Kuna see on variatsioon, hõlmab reaktsiooni entalpia arvutamine produktide entalpia lahutamist reagentide entalpiast:
∆H = HFOR - HR
Entalpia variatsiooni arvutamine võimaldab meil tuvastada, kas reaktsioon on endotermiline või eksotermiline. Kui tulemus on negatiivne, on reaktsioon eksotermiline; kui tulemus on positiivne, on reaktsioon endotermiline.
∆H = – (eksotermiline)
∆H = + (endotermiline)
Reaktsiooni entalpia variatsiooni arvutamisel on väga oluline, et oleme väga pöörake tähelepanu tasakaalule, kuna harjutuse poolt pakutavad entalpia väärtused on alati väljendatud mol. Seega, kui reaktsioonis osalejal on rohkem kui üks mool, peame korrutama selle entalpia väärtuse tasakaalus väljendatud kogusega. Vaadake näidet:
Ära nüüd lõpeta... Peale reklaami on veel midagi ;)
2 ZnS + 3 O2 → 2 ZnO + 2 SO2
Jälgime, et võrrandit tasakaalustavad koefitsiendid on 2, 3, 2 ja 2. Seega on iga osaleja entalpia väärtused:
HZnS = - 49,23. 2 = -98,46 Kcal/mol
HO2 = 0. 3 = 0 Kcal/mol
HZnO = - 83,24. 2 = -166,48 Kcal/mol
HSO2 = - 70,994. 2 = -141 988 Kcal/mol
Nende andmete põhjal saame arvutada reaktsiooni entalpia variatsiooni. Tasub meeles pidada, et toodete ja reaktiivide väärtused tuleb liita:
∆H = HFOR - HR
∆H = [(-166,48) + (-141,998)] - [(-98,46) + 0]
∆H = (-308,468) - (-98,46)
∆H = -308,468 + 98,46
∆H = -210,008 Kcal/mol
MÄRKUS. Kuna tulemus oli negatiivne, on see reaktsioon eksotermiline.
Nüüd järgige reaktsiooni entalpia arvutamisel vestibulaarse harjutuse resolutsiooni:
(UFMS) Alloleva tasakaalustatud võrrandi H väärtus on: Andmed: HAg2S = -32,6 KJ/mol, HH2O = -285,8 KJ/mol, HH2S = -20,6 KJ/mol,
2 Ag2S + 2 H2O → 4 Ag + 2 H2S + O2
a) 485,6 KJ
b) 495,6 KJ
c) 585,6 KJ
d) 595,6 KJ
e) 600 KJ
Harjutuste poolt edastatavad andmed on järgmised:
MÄRKUS. Kuidas meil on O2 võrrandis, mis on hapniku kõige stabiilsem allotroop, on selle entalpia 0 KJ. Kuna Ag on lihtaine, on selle entalpia väärtus 0 KJ.
HAg2S = -32,6 KJ/mol
HH2O = -285,8 KJ/mol
HH2S = -20,6 KJ/mol
Võttes arvesse tasakaalu, peame korrutama koefitsiendi iga osaleja entalpiaga:
HAg2S = - 32,6. 2 = -65,2 KJ
HH2O = - 285,8. 2 = -571,6 KJ
HH2S = - 20,6. 2 = -41,2 KJ
HO2 = 0. 1 = 0 KJ
HAg = 0. 4 = 0 KJ
Lõpuks kasutage lihtsalt entalpia variatsiooni valemis olevaid andmeid:
∆H = HFOR - HR
∆H = [(0) + (-41,2) + 0] - [(-65,2) + (-571,6)]
∆H = (-41,2) - (-636,8)
∆H = -41,2 + 636,8
∆H = 595,6 Kcal/mol
Kuna variatsiooni tulemus oli positiivne, on reaktsioon endotermiline.
Mina. Diogo Lopes Dias
Keemia

Termokeemia, entalpia, eralduv soojus, eksotermiline reaktsioon, põlemisreaktsioon, väliskeskkond, endotermiline reaktsioon, reaktsioon keemia, energiavahetus, reaktiivid, valguse emissioon, valguse neeldumine, soojus, elekter, komponendid, füüsikaline olek, tooted.