Keemine on muutus vedelast gaasiliseks olekuks. See juhtub siis, kui teatud rõhu all olev vedeliku osa saab soojust ja jõuab teatud temperatuurini.
Soojuse hulk, mida keha peab saama, et end täielikult auruks muuta, sõltub ainest, mis selle moodustavad.
Vedelas olekus ei ole määratletud vormi, eeldades seda sisaldava anuma kuju.
Olles praktiliselt arusaamatu, esitab see ühtlustava jõu seda moodustavate osakeste vahel.
Gaasilisse olekusse ülekandmiseks peab aine saama soojust. See energia suurenemine paneb molekulid suurema intensiivsusega vibreerima, suurendades nende vahelist kaugust.
Nii muutub ühtekuuluv jõud praktiliselt olematuks. Sellises olekus oleval kehal pole kindlat kuju ega mahtu.
Geisrid on näited keemisest, mis toimub vulkaanilistes piirkondades asuva põhjaveega. Magma soojendab vett ja teatud temperatuurini jõudes hakkab see olekut muutma.
Aur hõivab suurema mahu, suurendades rõhku maa-aluses õõnsuses. Selle tulemusena väljutatakse väikeste pragude kaudu pinnale auru ja vedeliku segu.

Keetmise omadused
Vedelik keeb järgmise mustri järgi:
- Hoides rõhku konstantsena, jääb temperatuur kogu keemisprotsessi jooksul konstantseks.
- Soojuse hulka massiühiku kohta, mis on vajalik vedeliku täielikuks auruks muundamiseks, nimetatakse varjatud auruks. Selle väärtus sõltub ainest, millest vedelik koosneb.
- Iga aine keemistemperatuur on hästi määratud ja seda nimetatakse keemistemperatuuriks.
Näpunäide: Toidu valmistamisel on hea, kui vesi keema hakkab, kuumus madalaks keerata. Kuna temperatuur püsib kogu keemisprotsessi vältel konstantsena, on küpsetusaeg kõrge kuumuse või väikese kuumusega sama. Nii säästame gaasi ja keskkond on tänulik.
Varjatud soojuse kogus
Soojuse hulk, mida vedelik peab auruks muundumiseks saama, sõltub varjatud aurustumissoojuse väärtusest ja massist.
Allpool esitame mõnede ainete varjatud aurustumissoojuse väärtuse:

Valem
Vedeliku oleku muutmiseks vajaliku soojushulga arvutamiseks kasutame järgmist valemit:
Kus
Qv: soojushulk (lubi)
m: mass (g)
Lv: varjatud aurustumissoojus (cal / g)
Näide:
Kui palju soojust on vaja 100 g etanooli keetmiseks ja täielikult auruks muutumiseks?
Qv = 100. 204 = 204 000 kal
Keemistemperatuur
Temperatuur, mille juures keha keeb, sõltub selle moodustavast ainest ja rõhust.
Ainete keemistemperatuur määratakse laboris. Näiteks on 1 atmosfääris oleva vee keemistemperatuur 100 ° C. Raud on 2800 ºC ja vesinik - 252,8 ºC.
Lugege ka teiste ainete faasimuutuse temperatuuri teadmiseks keemispunkt.
Mida väiksem on keha surve, seda madalam on selle keemistemperatuur. See tähendab, et suure kõrgusega linnades võtab toidu valmistamine palju kauem aega.
Toidu kiiremaks valmistamiseks kasutame kiirkeedukatte. Seda tüüpi pliit kasutab tihendussüsteemi, mis muudab selle sees oleva rõhu atmosfäärirõhust suuremaks.
Kõrgem rõhk muudab ka keemistemperatuuri kõrgemaks. Vee korral keeb see temperatuuril, mis võib ulatuda 120 ºC-ni, vähendades küpsetusaega.
faasimuutused
Üleminekut vedelast olekust gaasiliseks nimetatakse üldjuhul aurustamine, kuna see hõlmab lisaks keetmisele veel kahte protsessi: aurustumine ja küte.
Aurustamine toimub järk-järgult, selleks ei pea ilmtingimata saavutama kindlat temperatuuri. Teisest küljest toimub kuumutamine, kui asetame vedeliku pinnale, mille temperatuur on üle selle keemistemperatuuri.
Olekumuutustes on veel muid protsesse. Kas nad on:
- Fusioon
- Tahkumine
- Veeldamine või kondenseerumine
- Sublimatsioon
Alloleval diagrammil esindame neid kolme aine füüsikalised olekud ja vastavad oleku muutused:
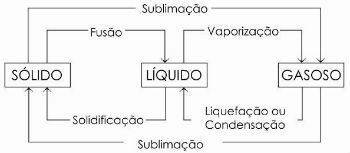
Lisateabe saamiseks lugege ka Vee füüsikalised olekud.
Harjutused
Vaenlane - 1999
Teksti tuleks kasutada kahe järgmise küsimuse jaoks.
Survepliit võimaldab toitu vees küpsetada palju kiiremini kui tavalised pliidid. Selle kaanel on kummist tihend, mis ei lase aurul välja pääseda, välja arvatud keskava kaudu, millele toetub rõhku kontrolliv raskus. Kasutamisel tekib seestpoolt kõrgrõhkkond. Selle ohutuks kasutamiseks on vaja jälgida keskava auku puhtust ja kaitseklapi olemasolu, mis tavaliselt asub kaanel.
Survekatla skeem ja veefaasi diagramm on esitatud allpool.
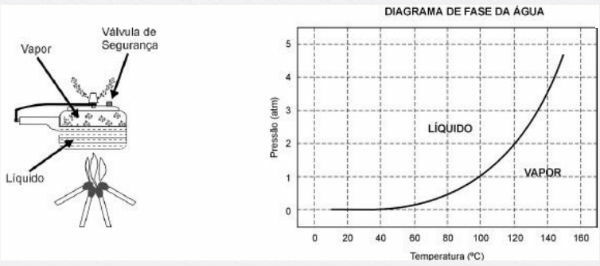
1) Survekatla kasutamise eeliseks on toidu valmistamise kiirus ja see on tingitud
a) rõhk selle sees, mis on võrdne rõhuga väljaspool.
b) selle siseruumide temperatuur, mis on üle koha vee keemistemperatuuri.
c) pannile ülekantava lisakütte kogus.
d) auru hulk, mille ventiil eraldab.
e) selle seina paksus, mis on suurem kui tavalistel pannidel.
Alternatiiv b: selle sisetemperatuuril, mis on üle selle koha keemistemperatuuri.
2) Kui säästlikkuse huvides vähendame kuumust kiirkuumutuspliidi all niipea, kui aur väljub klapi kaudu, et lihtsalt keemisaega, küpsetusaega hoida
a) see on suurem, sest pann “jahtub”.
b) on väiksem, kuna see vähendab veekadu.
c) on rõhu langedes suurem.
d) on suurem, kui aurustumine väheneb.
e) ei muutu, kuna temperatuur ei muutu.
Alternatiiv e: ei muudeta, kuna temperatuur ei varieeru.