O Thomsoni aatomimudel pakkus välja 1898. aastal inglise füüsik Joseph John Thomson või lihtsalt J. J. Thomson. Pärast mitu eksperimentaalsed tõendid elektroni olemasolu kohta, lükkas ta ümber pakutud teooria aatomi jagamatusest John Dalton.
Thomson kinnitas ja tõestas oma mudeli põhjal selle olemasolu elektronid (negatiivse elektrilaenguga osakesed) aatomis, see tähendab, et aatomil on subatoomilised osakesed.
Meelekaart: Thomsoni aatomimudel
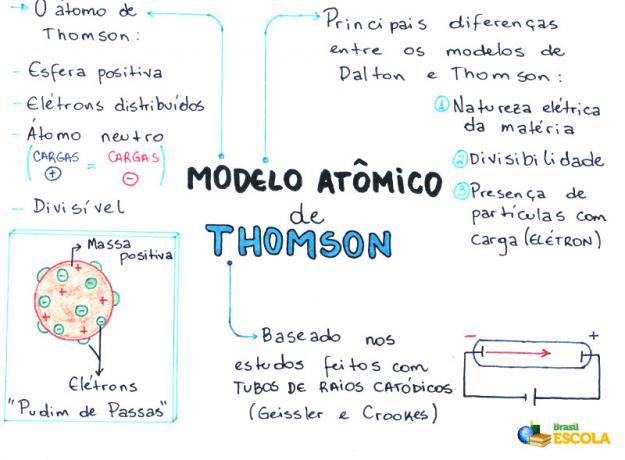
* Mõttekaardi allalaadimine PDF-failina Kliki siia!
Thomson pakkus välja oma aatomimudeli põhineb radioaktiivsusega seotud avastustel ja teadlaste Geissleri ja Crookesi ehitatud katoodkiiretorul läbi viidud katsetel. Vaadake selle toru kujutist:
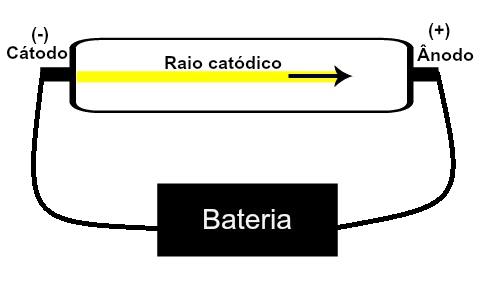
Kui haruldane, madalrõhugaas allutatakse kõrgele elektrilisele pingele (nt 15000 V), tekitab see a valgusvihk (koosneb elektrilaengutest) katoodist (negatiivne poolus) anoodi (poolus) suunas positiivne).
Selle eksperimendiga jõudis Thomson järeldusele, et kui gaasilise materjali aatomid sees toru allutati kõrgepingele, nende elektronid rebiti välja ja suunati plaadile positiivne.
Thomsoni aatomimudeli pakutud kaalutlused
Katoodkiiretoruga läbi viidud katsetega pakkus Thomson välja oma tõlgenduse selle kohta, milline oleks aatom ja selle koostis. Nii et tema sõnul:
- Aatom on sfäär, kuid mitte massiivne, nagu pakub välja John Daltoni aatomimudel;
- Aatom on neutraalne, kuna kogu aine on neutraalne;
- Kuna aatomil on elektronid, millel on negatiivsed laengud, peavad sellel olema positiivsed osakesed, nii et lõplik laeng oleks null;
- Elektronid pole aatomis fikseeritud ega kinni jäänud, neid saab teatud tingimustel teisele aatomile üle kanda;
- Aatomit võib pidada positiivse laenguga pidevaks vedelikuks, kus jaotuksid negatiivse laenguga elektronid;
- seotud teie modelleerida rosinapudingule (mis esindavad elektrone);
- Kuna hajutatud elektronidel on sama laeng, toimub nende vahel vastastikune tõrjumine, mis muudab need sfääris ühtlaselt jaotatuks.
Thomsoni mudeli abil aatomile välja pakutud uudsused
Teiseks pakuti aatomi jaoks välja Thomsoni aatomimudel. Esimese mudeli sõnastas John Dalton.
Ärge lõpetage kohe... Peale reklaami on veel;)
Thomsoni mudel käsitles uusi teadmisi aatomi kohta, mida seni teadusliku aluse puudumise tõttu välja ei pakutud, näiteks:
- Aine elektriline olemus;
- Aatomi jagatavus;
- Väikeste laetud osakeste olemasolu aatomis.
Thomsoni aatomile osutasid probleemid
Mitu füüsikut ettepaneku esitamise ajal Thomsoni aatomimudel, mis põhineb klassikalise füüsika teooriatel, tõi välja mõned selles mudelis esinevad vastuolud:
- Thomson pakkus, et aatomil on elektronide ühtlase jaotuse suhtes stabiilsus, mida saab energia mõjul muuta. Kuid klassikaline füüsika, mis põhineb elektromagnetism, ei võimalda stabiilse süsteemi olemasolu, mis põhineb ainult sama laenguga osakeste vahelisel tõrjumisel;
- Thomsoni jaoks jaotuvad elektronid aatomis ühtlaselt, kuid neil on võime seda teha kiirendatud viisil ja seetõttu peab see teatud sagedustel kiirgama elektromagnetilist kiirgust spetsiifiline. Seda aga ei täheldatud.
- Thomsoni mudel oli aatomite omaduste, näiteks nende koostise ja korralduse, selgitamisel sageli ebaefektiivne.
* Victor Ricardo Ferreira mõttekaart
Keemiaõpetaja
Minu poolt. Diogo Lopes Dias
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
PÄEVAD, Diogo Lopes. "Thomsoni aatomimudel"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/o-atomo-thomson.htm. Juurdepääs 27. juunil 2021.
Keemia

Niels Bohr, Bohri aatom, aatomifüüsika, stabiilne aatom, aatomimudel, planeedisüsteem, elektrosfääri kihid, energiatasemed, elektronkestad, elektronenergia, Rutherfordi aatomimudel, ergastatud oleku aatom.
Keemia
Aatomid ja Universumi ehitus, aatomiteooria, et kõik on tehtud, aine koosneb aatomitest, nelja elemendi teooria, iidsed alkeemikud, aatomiteooria, põhiosake.