Mateeria võib läbida kahte peamist transformatsioonitüüpi, füüsikalised ja keemilised. Füüsiline muundumine on siis, kui aine olemust ei muudeta, see tähendab selle koostis. Näiteks kui me tükeldasime puidutükki, siis see muutus, kuid see oli füüsikaline nähtus, sest see on ikkagi puit, selle koostis on sama, mis alguses.
Teiselt poolt, keemiline muundumine või nähtus toimub aine olemuse või koostise muutmisel. Sellisel juhul on algosakesed (milleks võivad olla molekulid, aatomid, ioonkobarad, ioonid jne) nagu lahti ja nende aatomid korraldavad end ümber, moodustades uusi molekule, klastreid, aatomeid, ioone jne, see tähendab uusi aineid. See on keemiline reaktsioon.
Kujutage näiteks ette, et toome etüülalkoholi lähedale valgustatud tikutopsi. Me teame, mis juhtub: alkohol hakkab põlema. See tähendab, et sellel toimub keemiline reaktsioon õhus oleva hapnikuga (O2) ja muudab selle koostist, mis ei ole enam etanool (C2H6O) ja ka hapnikul pole enam oma esialgset koostist, mis pärsib uusi aineid, milleks on süsinikdioksiid (CO2) ja vesi (H2O).

Alkohol tulekahjus - põlemisreaktsioon
Keemilistes reaktsioonides nimetatakse lähteaineid reaktiivid ja lõpp tootedja reaktsioonid on esindatud läbi keemilised võrrandid, mis järgivad järgmist üldstruktuuri:
REAKTIIVID → TOOTED
Võttes arvesse alkoholi (etanooli) täieliku põlemisreaktsiooni eelmist näidet, on meil järgmine keemiline võrrand:
Etanool + gaasihapnik → Süsinikdioksiid + vesi
Seda keemilist reaktsiooni on allpool kujutatud aatomite abil vastavalt Daltoni mudelile lihtsate sfääride kujul:
Ärge lõpetage kohe... Peale reklaami on veel;)
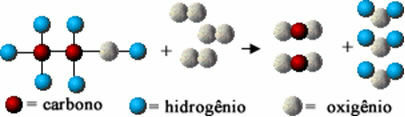
Etanooli põlemisreaktsiooni mudeli esitus
Pange tähele, et esialgsed sidemed aatomite vahel katkesid ja need moodustasid uued sidemed ning ilmusid uued ained.
Seega kirjutatakse keemilised võrrandid valemite ja sümbolite abil, mis kõige paremini esindavad ülaltoodud skeemi. Vaadeldaval juhul (etanooli põlemisreaktsioon) on keemiline võrrand väljendatud järgmiselt:
Ç2H5oh(?) + 3 O2 g) → 2 CO2 g) + 3 H2Ov)
Keemilise reaktsiooni ilmnemist näitavad mõned visuaalsed tegurid:
* Gaasi vabastamine;
* Värvi muutus;
* Sademete moodustumine;
* Leegi välimus või heledus.
Olulised protsessid, mis toimuvad meie kehas, looduses ja tööstuses, näiteks ravimite ja tööstuslike toiduainete tootmine, on keemilised reaktsioonid. Seetõttu on need elu tekkimiseks ja säilitamiseks äärmiselt olulised.
Keemilisi reaktsioone on mitut tüüpi, mida saab klassifitseerida vastavalt erinevatele kriteeriumidele, kuid peamised keemias uuritavad tüübid on:
1. Anorgaanilised reaktsioonid: Need klassifitseeritakse tavaliselt vastavalt moodustunud ainete arvule, reagentide arvule ning lihtsate ja liitainete olemasolule või puudumisele. Anorgaanilisi reaktsioone on neli peamist tüüpi:
1.1. Sünteesi- või liitumisreaktsioonid;
1.2. Lagunemis- või analüüsireaktsioon;
1.3. Lihtne vahetamine, nihutamine või redoksreaktsioon;
1.4. Topeltvahetus ehk metateesireaktsioon;
2. Orgaanilised reaktsioonid: Need hõlmavad süsinikuühendeid. Need liigitatakse tavaliselt kolme põhitüüpi:
2.1. Liitmisreaktsioonid;
2.2. Asendusreaktsioonid;
2.3. Likvideerimisreaktsioonid.
Autor Jennifer Fogaça
Lõpetanud keemia
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FOGAÇA, Jennifer Rocha Vargas. "Mis on keemiline reaktsioon?"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-reacao-quimica.htm. Juurdepääs 28. juunil 2021.
Mis on keemia?

Mõistke, mis on Kp, tasakaalukonstant rõhu osas, ja tea, kuidas seda rõhkude abil saada osakesed kõikidest keemilises tasakaalus olevatest gaasidest, mis võivad olla atmosfääris (atm) või millimeetrites elavhõbedas (mmHg). Klõpsake siin ja saate selle teema kohta rohkem teada!