isómero geométrico Es un tipo de isomería espacial que evalúa y compara la posición en el espacio de los ligandos de dos átomos de carbono en una cadena. Esta evaluación se realiza a partir de un plano imaginario entre los carbonos involucrados.
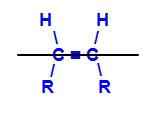
Plano imaginario que divide la molécula.
El plano imaginario en la estructura de arriba divide la molécula en un plano superior y un plano inferior. Con esto, podemos evaluar y comparar los ligandos de carbono involucrados en cada uno de estos planos. Vea los tipos de isómeros geométricos:
→ Isómero geométrico cis-trans
Un compuesto tiene isomería geométrica cis-trans cuando la cadena muestra:
Cadena abierta con un doble enlace entre dos carbonos, que tienen los mismos enlaces entre sí. Vea un ejemplo:
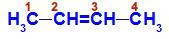
Fórmula estructural de But-2-eno
En la estructura, podemos observar que tanto el carbono 2 como el carbono 3 tienen los mismos ligandos, que son hidrógeno (H) y metilo (CH3).
Cadena cerrada con dos carbonos que tienen los mismos ligandos entre sí. Vea un ejemplo:
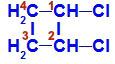
Fórmula estructural del 1,2-dicloro-ciclobutano
En la estructura, podemos observar que tanto el carbono 1 como el carbono 2 tienen los mismos ligandos, que son hidrógeno (H) y cloro (Cl).
Para explicar la isomería cis-trans, usaremos but-2-eno:
a) Isómero cis: es el isómero geométrico en el que los mismos ligandos ocupan el mismo plano. En el siguiente ejemplo, los hidrógenos están en el mismo plano, al igual que los radicales metilo.

Fórmula estructural de cis-but-2-eno
b) Isómero trans: es el isómero geométrico en el que diferentes ligandos ocupan el mismo plano. En el siguiente ejemplo, tenemos en el mismo plano un hidrógeno y un metilo (CH3).
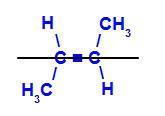
Fórmula estructural de trans but-2-eno
No pares ahora... Hay más después de la publicidad;)
→ Isómero geométrico E-Z
Un compuesto tiene isomería geométrica E-Z cuando la cadena tiene:
Cadena abierta con un doble enlace entre dos carbonos, que tienen todos o algunos enlazadores diferentes. Vea un ejemplo:
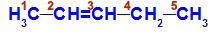
Fórmula estructural de pent-2-eno
En la estructura, podemos ver que el carbono 2 tiene el ligando de metilo (CH3) e hidrógeno (H), y el carbono 3 tiene el ligando de hidrógeno (H) y etilo (H)3C-CH2).
Cadena cerrada con dos carbonos que tienen todos o algunos ligandos diferentes entre sí. Vea un ejemplo:
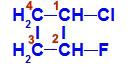
Fórmula estructural de 1-cloro-2-fluoro-ciclobutano
En la estructura, podemos observar que el carbono 1 tiene hidrógeno y cloro como ligandos principales, y el carbono 2 tiene hidrógeno y flúor como ligandos principales.
NOTA: Entre los diferentes ligandos, en isomería geométrica, evaluamos la complejidad del ligando (número de átomos) o el número atómico.
Para explicar el isómero E-Z, usaremos tanto pent-2-eno como 1-cloro-2-fluoro-ciclobutano:
a) E-isómero
isómero geométrico en el que los ligandos más complejos o de mayor número atómico se colocan en planos opuestos. En el siguiente ejemplo, el ligando más complejo en el carbono 2 es metilo y el ligando más complejo en el carbono 3 es etilo, que se colocan en diferentes planos.
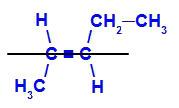
Fórmula estructural de E-pent-2-eno
b) Isómero Z
isómero geométrico en el que los ligandos más complejos o los de mayor número atómico se colocan en el mismo plano. En el siguiente ejemplo, el ligando de mayor número atómico del carbono 1 es el cloro (Z = 17), y el ligando de mayor número atómico del carbono 2 es el flúor (Z = 9), que se colocan en el mismo plano.
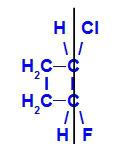
Fórmula estructural de Z-1-cloro-2-fluoro-ciclobutano
Por mí. Diogo Lopes Dias
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
DÍAS, Diogo Lopes. "¿Qué es la isomería geométrica?"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria-geometrica.htm. Consultado el 28 de junio de 2021.
Química
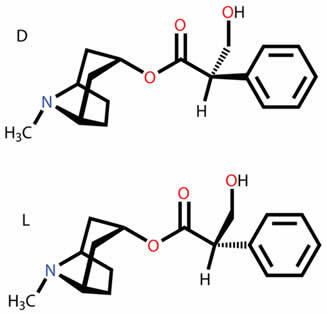
Sepa de qué se tratan los diversos tipos de isómeros planos y espaciales, como función, posición, cadena, tautomería, metamerismo, isomería cis-trans geométrica y óptica.