Hay cuatro factores principales que cambian la velocidad de las reacciones, mira cuáles son:
1-Superficie de contactoO:Cuanto mayor sea la superficie de contacto, mayor será la velocidad de reacción.
Esto se debe a que las reacciones tienen lugar entre las moléculas que se asientan en las superficies de los reactivos. Realizan colisiones que, de ser efectivas (con la orientación correcta y con la cantidad de energía necesario), resultará en la ruptura de enlaces antiguos y la formación de nuevos, es decir, la reacción química ocurrira. Por lo tanto, cuanto mayor sea la superficie de contacto, más moléculas estarán en contacto entre sí, más probabilidades habrá de que se produzcan choques efectivos y más rápida será la reacción.
Un ejemplo que lo confirma es si reacciona con la misma cantidad de agua una tableta efervescente entera y una triturada. ¿Cuál terminará reaccionando más rápido? La respuesta es la tableta triturada, ya que su superficie de contacto es mucho más grande que la de la tableta compacta.

Reacción entre el antiácido efervescente y el agua en dos situaciones diferentes: en el primer vaso, el antiácido se pulveriza; en el segundo, está en tableta
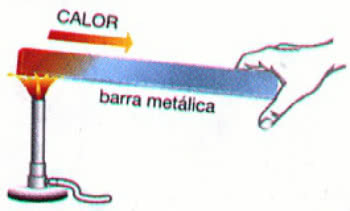
2- Temperatura:Cuanto mayor sea la temperatura, más rápida será la reacción.
Esto sucede porque, con el aumento de temperatura, aumenta la energía cinética de las moléculas de las sustancias reaccionantes, es decir, se mueven a mayor velocidad, lo que aumenta la cantidad de choques efectivos que resultan en una mayor rápido. Además, a medida que aumenta la energía de las moléculas, esto les permite tener suficiente energía para reaccionar, lo que se denomina energía de activación.
Por ejemplo, cuando ocurre un incendio en un bosque, que es un medio donde la pérdida de calor es pequeña, la reacción libera calor en el medio. Como resultado, la temperatura del ambiente aumenta y esto hace que la reacción de combustión tenga lugar aún más rápido.

El aumento de temperatura aumenta aún más la velocidad de los incendios forestales
La olla a presión también se utiliza para este fin, ya que el aumento de presión aumenta la temperatura a la que hierve el líquido y, en consecuencia, más rápida es la cocción de los alimentos.

La olla a presión es un ejemplo de la influencia de la temperatura en la velocidad de reacción.
No pares ahora... Hay más después de la publicidad;)
Por otro lado, si queremos que la reacción sea más lenta, podemos bajar la temperatura. Es el caso que ponemos, por ejemplo, carne en el congelador, ya que la baja temperatura hace que este alimento se descomponga más lentamente.
3- Concentración:Cuanto mayor sea la concentración de reactivos, mayor será la velocidad de reacción.
Cuando aumentamos la concentración de reactivos, aumentamos el número de moléculas o partículas que reaccionan por unidad. de volumen y, en consecuencia, aumenta el número de colisiones entre ellos, lo que se traduce en una mayor velocidad de reacción.
Un ejemplo es la combustión de carbón. Si ponemos un trozo de carbón al rojo vivo en un matraz de oxígeno puro, la reacción procederá mucho más rápido. Esto se debe a que ha aumentado la concentración de uno de los reactivos de combustión (oxígeno). Antes, el oxígeno estaba presente en el aire, que está en una proporción de aproximadamente el 20%. Dentro de la botella, sin embargo, esta proporción llega al 100%.
4- Catalizadores: Son sustancias que aumentan la velocidad de determinadas reacciones sin participar en ellas, es decir, sin ser consumidas durante la reacción.
Por ejemplo, el peróxido de hidrógeno se descompone con el tiempo, pero cuando entra en contacto con la sangre de una lesión, esta reacción se produce con una velocidad mucho mayor, que se ve a través de la formación de burbujas.
Esto sucede porque la sangre tiene una enzima llamada catalasa que actúa como catalizador de la reacción de descomposición del peróxido de hidrógeno, es decir, aumenta su velocidad.
Los catalizadores pueden aumentar la velocidad de las reacciones porque actúan cambiando el mecanismo de reacción al disminuir la energía de activación de la reacción. Por lo tanto, con una cantidad menor de energía de activación, es más fácil que las partículas en reacción alcancen esta energía y reaccionen.
Comprenda mejor cómo sucede esto leyendo el texto Cómo funcionan las sustancias catalizadoras.
Hay otros factores que pueden interferir con reacciones específicas. Algunos ejemplos son: luz,electricidad, presión (en el caso de sistemas gaseosos) y naturaleza de los reactivos (Cuanto mayor sea el número de enlaces reactivos que deben romperse y cuanto más fuertes sean, más durará la reacción).
Por Jennifer Fogaça
Licenciada en Química