Tú rieles son elementos químicos que presentan como principal característica física la capacidad de perder electrones y, en consecuencia, formar cationes metálicos. Por esta razón, pueden formar dos tipos de enlaces químicos: el enlace iónico y el enlace metálico.
LA enlace iónico ocurre cuando un metal interactúa con un elemento de naturaleza metálica, que puede ser un un metal o hidrógeno. En este tipo de enlace, tenemos la pérdida de electrones por los metales y la ganancia de electrones por los no metales o el hidrógeno.
ya el enlace metálico se establece entre los átomos de un solo elemento metálico. Este tipo de enlace ocurre solo entre los átomos de un solo metal y exclusivamente porque un metal no puede establecer un enlace químico con otro elemento metálico diferente.
Características generales de los metales.
Sólidos a temperatura ambiente, a excepción del mercurio;
Son brillantes;
Tienen altos puntos de fusión y ebullición;
Generalmente son de color plateado, a excepción del oro, que es dorado, y el cobre, que es rojizo;
Los metales puros están formados por grupos de átomos (de un solo elemento químico) llamados redes cristalinas.
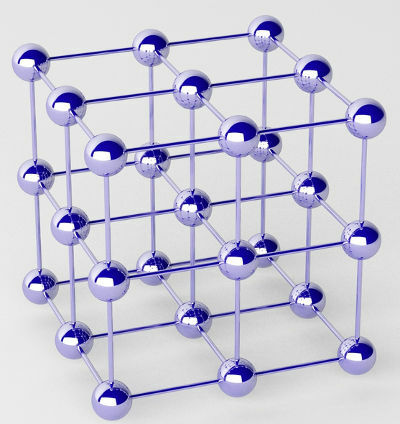
Representación de la red cristalina de un metal.
Principios de la unión metálica
A enlace metálico, las redes cristalinas que forman los metales son en realidad un grupo iónico (compuesto solo de cationes y electrones). Los electrones presentes en la capa de valencia de los átomos metálicos se deslocalizan, es decir, abandonan la capa de valencia, provocando que el átomo se convierta en un catión (deficiente en electrones).
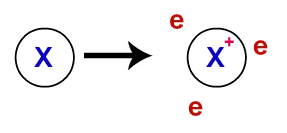
Representación de electrones deslocalizados de la capa de valencia
Después de ser deslocalizados, los electrones de los átomos de metal comienzan a rodear los cationes, formando un verdadero "mar de electrones". Cada uno de los electrones presentes en este mar tiene la capacidad de moverse libremente a través de la red cristalina del metal.

Representación del modelo del mar de electrones
NOTA: Los electrones "del mar" no pueden salir de la red cristalina y moverse a través de ella.
Propiedades de los metales justificadas por enlaces metálicos.
a) maleabilidad
A través de un metal, es posible producir láminas de diferentes espesores y láminas. Es gracias a esta propiedad de los metales que podemos construir diversos objetos, como cuchillos, espadas, etc.

La hoja de una espada está hecha de metal.
b) Conductividad
Los metales, en general, son buenos conductores de corriente eléctrica y calor. Cuando cualquier metal está en contacto con una fuente de calor o una fuente de corriente eléctrica, es capaz de conducirlos.

Una sartén de aluminio en la llama de una estufa se calienta por completo debido a la conductividad.
c) Ductibilidad
A través de un metal, podemos producir alambres. El uso de un metal en forma de alambres facilita su uso, especialmente en relación a la conductividad eléctrica.

Se puede utilizar un metal, como el cobre, para producir alambres.
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ligacao-metalica.htm