La ionización es una reacción química que origina iones a partir de sustancias moleculares colocadas en el agua.
Entonces, podemos decir que la ionización es la proceso deformación de iones.
Los ácidos son ejemplos de sustancias que sufren ionización cuando se colocan en agua.
proceso de ionización
Vea cómo ocurre el proceso de ionización a través del siguiente ejemplo:
Cuando se coloca en agua, el ácido clorhídrico (HCl) sufre ionización. El enlace químico entre H y Cl se rompe y se forman iones H+ y Cl-, que están rodeados de agua.
Como hemos visto, la H+ perdió un electrón y el Cl- recibió un electrón. Sin embargo, la H+ necesita estabilizarse y, por lo tanto, se une al agua.
Por lo tanto, la reacción de ionización de HCl también se puede representar de la siguiente manera:
Ahora observamos la formación del catión hidronio (H3O+), resultado de la unión de la H+ y de H2O.
También es importante señalar que en este ejemplo, Cl recibe el electrón porque es el más electronegativo, es decir, tiene tendencia a ganar electrones. Por lo tanto, atrajo fácilmente los electrones hacia sí mismo.
Lea también:
- electrones
- ion, catión y anión
- Reacción química
Vea otros ejemplos de ionización:
1)
2)
LA energía de ionización o potencial de ionización es una propiedad periódica que indica la cantidad de energía necesaria para transferir un electrón de un átomo en un estado fundamental.
Disociación e ionización
LA disociación es un fenómeno físico, no una reacción química. Se refiere a la liberación de iones existentes de compuestos iónicos en el agua.
La principal diferencia entre disociación e ionización es:
- Ionización: se forman iones;
- Disociación: los iones existentes se separan.
El proceso de disociación solo tiene lugar con sales y bases. Ejemplo: NaCl, sal de mesa.
La disociación y la ionización son procesos importantes para que se produzcan reacciones químicas, ya que los iones libres son más reactivos que las moléculas.
Lea también:
- Ácidos
- sales
- Bases
- equilibrio iónico
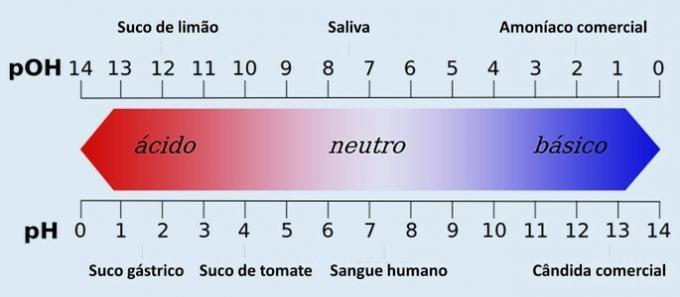
- Concepto y determinación de pH y pOH
- Reacción de neutralización
Asegúrese de consultar las preguntas del examen de ingreso sobre el tema, con una resolución comentada, en: ejercicios sobre funciones inorgánicas.