Base es una sustancia inorgánica que, según el químico sueco Svante Arrhenius, cuando se coloca en el agua, sufre el fenómeno de disociación iónica, en el que se produce el lanzamiento de iones: catión (Y+) y anión hidróxido (OH-).

Fórmula general de una base de Arrhenius
el grupo Y de un base puede ser cualquier metal o bien del grupo amonio (NH4+), que se liberan en el agua como cationes durante la disociación, como se puede apreciar en la ecuación que representa el proceso:
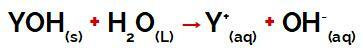
Ecuación que representa la disociación de una base.
Consulte a continuación información muy importante sobre la clasificación y nomenclatura de bases.
1) Clasificación respecto a la solubilidad de bases(habilidad para disolver en el agua)
Bases soluble: tener metal alcalino o amonio en la composición;
Bases escasamente soluble: tengo metal alcalinotérreo en composición. Ejemplo: hidróxido de magnesio, ampliamente utilizado como antiácido y laxante;
bases practicamente insoluble: tener cualquier otro metal en la composición. Ejemplo: hidróxido de aluminio, ampliamente utilizado como antiácido.
2) Clasificación respecto a la fuerza de base(habilidad para disociar en el agua)
Bases fuerte: tener metales alcalinos o alcalinotérreos, a excepción del magnesio, en la composición;
Bases débil: tener cualquier otro metal en la composición.
3) Nomenclatura base
Para nombrar una base, simplemente siga la regla de nomenclatura a continuación:
Hidróxido + de + nombre del metal o amonio
Ejemplo: Ca (OH)2 → hidróxido de calcio
Si la base tiene un elemento químico que no pertenece a las familias IA, IIA o IIIA (y que no es el plata o zinc), debemos indicar delante del nombre del elemento, en números romanos, el número de hidroxilos:
Ejemplo: Ti (OH)4 → hidróxido de titanio IV
Por mí. Diogo Lopes
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-base.htm
