La unión iónica se produce entre iones, como sugiere su nombre. Debido a que tienen cargas opuestas, los cationes (elemento con carga positiva) y los aniones (elemento con carga negativa) se atraen electrostáticamente entre sí, formando el enlace. Sin embargo, un sólido iónico está constituido por un aglomerado de cationes y aniones organizados con formas geométricas bien definidas, denominadas celosías o celosías cristalinas.
Por ejemplo, la sal (cloruro de sodio) se forma por la transferencia definitiva de un electrón del sodio al cloro, dando lugar al catión sodio (Na+) y el anión cloruro (Cl-). En la práctica, esta reacción involucra no solo dos átomos, sino un número enorme e indeterminado de átomos que forman una red cristalina de forma cúbica, como se muestra a continuación:
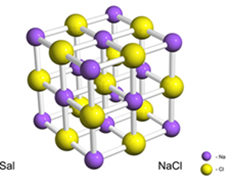
Si observamos los cristales de sal con un microscopio electrónico de barrido, veremos que en realidad son cúbicos debido a su estructura interna.

Dado que cada compuesto iónico está formado por un número indeterminado y muy grande de iones, ¿cómo podemos representar un compuesto iónico?
La fórmula que se utiliza habitualmente es la fórmula unitaria, que es el que representa la proporción expresada por el menor número posible de cationes y aniones que componen la red cristalina, de modo que se neutraliza la carga total del compuesto. Para que esto suceda, es necesario que el número de electrones entregados por un átomo sea igual al número de electrones recibidos por el otro átomo.
Algunos aspectos sobre la fórmula unitaria de los compuestos iónicos son importantes, vea algunos:
- Escriba siempre el catión primero y luego el anión;
- Dado que cada compuesto iónico es eléctricamente neutro, no es necesario anotar las cargas de los iones individuales;
- Los números de subíndice que aparecen en el lado derecho de cada ion indican la proporción de átomos del catión al anión. Estos números se denominan índices y el número 1 no está escrito.
Por ejemplo, en el caso del cloruro de sodio, tenemos que su fórmula unitaria es NaCl, ya que tenemos exactamente 1 catión de sodio por cada anión de cloruro.
Vea otro ejemplo, Al3+ tiene tres cargas positivas, mientras que la F- solo tiene un negativo, por lo que se necesitan tres aniones fluoruro para neutralizar el compuesto. Por lo tanto, concluimos que su fórmula unitaria es AlF3.
Una forma sencilla de llegar a la fórmula unitaria del compuesto iónico es intercambiar sus cargas por sus índices, como se muestra de forma genérica a continuación:
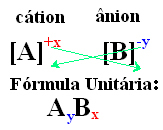
Ejemplos:

Otra fórmula utilizada para representar sustancias iónicas es la Fórmula de Lewis o fórmula electrónica, qué representa los electrones de la capa de valencia de los iones "bolas" alrededor del símbolo del elemento. En el caso de la sal tenemos:

Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/formulas-para-representar-as-ligacoes-ionicas.htm

