LA Tabla periodica es un modelo que agrupa todos los elementos químicos conocidos y sus propiedades. Están dispuestos en orden ascendente de números atómicos (número de protones).
En total, la nueva tabla periódica tiene 118 elementos químicos (92 naturales y 26 artificiales).
Cada cuadrado especifica el nombre del elemento químico, su símbolo y su número atómico.
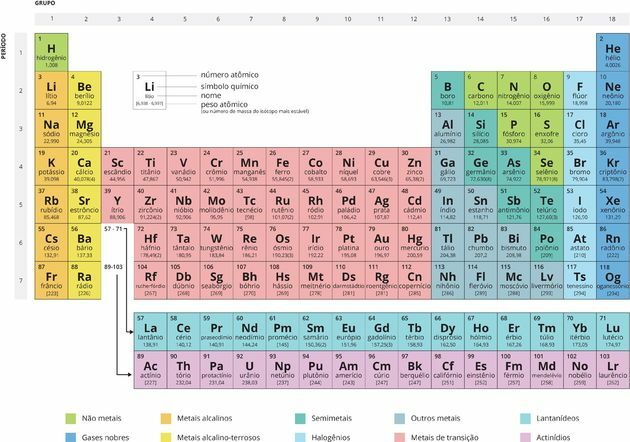
Organización de la tabla periódica
las llamadas Periodos son líneas horizontales numeradas, que tienen elementos que tienen el mismo número de capas electrónicas, totalizando siete períodos.
- 1 ° período: 2 elementos
- 2do período: 8 elementos
- 3er periodo: 8 elementos
- Cuarto período: 18 elementos
- 5to período: 18 elementos
- Sexto período: 32 elementos
- Séptimo período: 32 elementos
Con la organización de los períodos en la tabla, algunas líneas horizontales se volverían muy largas, por lo que es común representar la serie de lantánidos y la serie de actínidos aparte de las demás.
A Familias o grupos son las columnas verticales, donde los elementos tienen el mismo número de electrones en la capa más externa, es decir, en el
capa de valencia. Muchos elementos de estos grupos están relacionados según su propiedades químicas.Hay dieciocho Grupos (A y B), y las familias más conocidas son del Grupo A, también llamado elementos representativos:
- 1A familia: Metales alcalinos (litio, sodio, potasio, rubidio, cesio y francio).
- Familia 2A: Metales alcalinotérreos (berilio, magnesio, calcio, estroncio, bario y radio).
- Familia 3A: Familia del boro (boro, aluminio, galio, indio, talio y nihonio).
- Familia 4A: Familia del carbono (carbono, silicio, germanio, estaño, plomo y flerovio).
- Familia 5A: Familia del nitrógeno (nitrógeno, fósforo, arsénico, antimonio, bismuto y moscovia).
- Familia 6A: Calcógenos (oxígeno, azufre, selenio, telurio, polonio, hígado).
- Familia 7A: Halógenos (flúor, cloro, bromo, yodo, astato y tenessine).
- Familia 8A: Gases nobles (Helio, Neón, Argón, Criptón, Xenón, Radón y Oganessonio).
Tú elementos de transición, también llamados metales de transición, representan las 8 familias del Grupo B:
- Familia 1B: cobre, plata, oro y roentgen.
- Familia 2B: zinc, cadmio, mercurio y copérnico.
- Familia 3B: series de escandio, itrio y lantánidos (15 elementos) y actínidos (15 elementos).
- Familia 4B: titanio, circonio, hafnio y rutherfordio.
- Familia 5B: vanadio, niobio, tantalio y dubnio.
- Familia 6B: cromo, molibdeno, tungsteno y seaborgio.
- Familia 7B: manganeso, tecnecio, renio y bohrio.
- Familia 8B: hierro, rutenio, osmio, hasio, cobalto, rodio, iridio, meitnerio, níquel, paladio, platino, darmstadium.
Por determinación de la Unión Internacional de Química Pura y Aplicada (IUPAC), los grupos comenzaron a organizarse por números del 1 al 18, aunque todavía es común encontrar familias descritas por letras y números como se muestra arriba.
Una diferencia importante que generó el nuevo sistema presentado por IUPAC es que la familia 8B corresponde a los grupos 8, 9 y 10 de la tabla periódica.
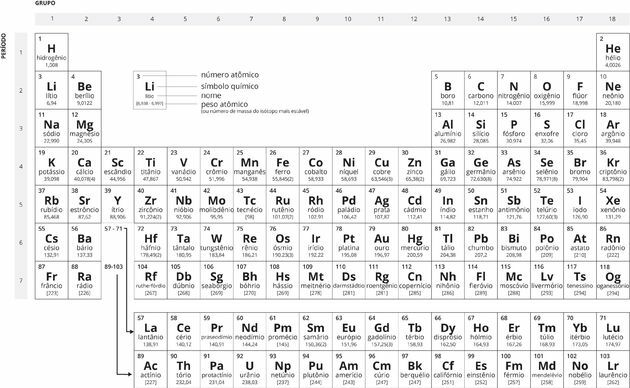
Tabla periódica en blanco y negro
Historia de la tabla periódica
El propósito fundamental de crear una tabla era facilitar la clasificación, organización y agrupación de elementos según sus propiedades.
Hasta llegar al modelo actual, muchos científicos crearon tablas que podrían demostrar una forma de organizar los elementos químicos.
La tabla periódica más completa fue elaborada por el químico ruso. Dmitri Mendeleev (1834-1907), en el año 1869 debido a la masa atomica de los elementos.
Mendeleev organizó grupos de elementos de acuerdo con propiedades similares y dejó espacios vacíos para los elementos que creía que aún serían descubiertos.
La tabla periódica como la conocemos hoy fue organizada por Henry Moseley, en 1913, por orden de número atómico elementos químicos, reorganizando la tabla propuesta por Mendeleev.
William Ramsay descubrió los elementos neón, argón, criptón y xenón. Estos elementos, junto con el helio y el radón, incluían la familia de los gases nobles en la tabla periódica.
Glenn Seaborg descubrió los elementos transuránicos (números 94 al 102) y en 1944 propuso la reconfiguración de la Tabla Periódica, colocando la serie de actínidos debajo de la serie de lantánidos.
En 2019, la tabla periódica cumple 150 años y se creó una resolución de Naciones Unidas y UNESCO para hacer de este el Año Tabla periódica internacional de elementos químicos como forma de reconocer una de las creaciones más influyentes e importantes de Ciencia.
Curiosidades de la tabla periódica
- La Unión Internacional de Química Pura y Aplicada Unión internacional de Química Pura Aplicada - IUPAC) es una ONG (organización no gubernamental) dedicada a estudios y avances en Química. A nivel mundial, la Organización recomienda el estándar establecido para la Tabla Periódica.
- Hace 350 años, el primer elemento químico aislado en el laboratorio fue el fósforo por el alquimista alemán Henning Brand.
- El elemento plutonio fue descubierto en la década de 1940 por el químico estadounidense Glenn Seaborg. Descubrió todos los elementos transuránicos y ganó el Premio Nobel en 1951. El elemento 106 fue nombrado Seaborgio en su honor.
- En 2016, se oficializaron los nuevos elementos químicos de la tabla: Tennessine (Ununséptio), Nihonium (Ununtrio), Moscovium (Ununpêntio) y Oganesson (Ununóctio).
- Los nuevos elementos químicos sintetizados se denominan superpesados porque contienen una gran cantidad de protones, que es muy superior a los elementos químicos que se encuentran en la naturaleza.
Resumen de la tabla periódica
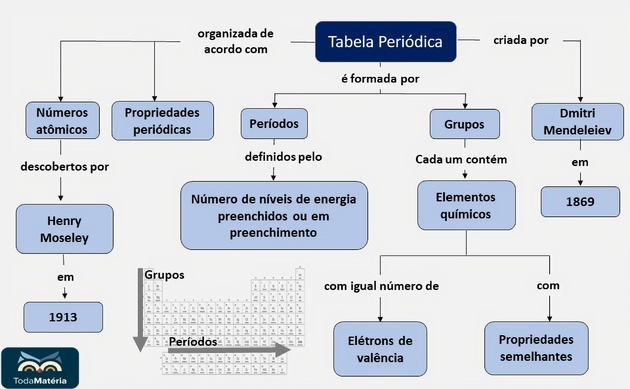
Verifique las preguntas del examen de ingreso con una resolución comentada en Ejercicios de la tabla periódica y preguntas inéditas en Ejercicios para organizar la tabla periódica.