
A veces le puede pasar a fórmula mínima ser la misma que la fórmula molecular del compuesto; sin embargo, esto no siempre es cierto.
Por ejemplo, la fórmula empírica o mínima para el agua es H2O, lo que indica que hay una proporción de 2: 1 entre los elementos que componen las moléculas de agua. Y, casualmente, esta también es la fórmula molecular del agua. Sin embargo, para ver que esto no siempre sucede, observe los dos ejemplos siguientes:
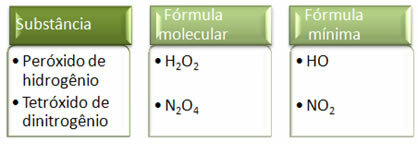
Dado que la fórmula mínima es solo la proporción de átomos de cada elemento y no la cantidad real de ellos en la fórmula molecular, puede ocurrir de diferentes compuestos que tienen la misma fórmula empírica e incluso la fórmula mínima de un compuesto puede ser la misma que la fórmula molecular de otro. Tenga en cuenta, en el ejemplo siguiente, cómo puede suceder esto:
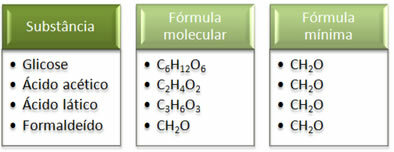
Ver que la fórmula mínima CH2El es el mismo para todas las sustancias, es decir, esta fórmula mínima expresa que, en todos los casos, la Los átomos de carbono, hidrógeno y oxígeno están presentes en fórmulas moleculares en una proporción de 1:2:1. Además, el único que tiene la misma fórmula molecular que la fórmula empírica es el formaldehído.
- Cálculo de fórmula mínima o empírica:
Para determinar la fórmula empírica de un compuesto, primero es necesario saber cuál es su porcentaje o fórmula aproximada. Esto se puede hacer midiendo la masa de cada elemento en 100 g de una muestra. El texto "Porcentaje o fórmula centesimal”Aclara mejor este asunto.
No pares ahora... Hay más después de la publicidad;)
Por ejemplo, digamos que la composición aproximada de un compuesto dado está dada por: 40,00% C, 6,67% H y 53,33% O. Pasamos estos valores a gramos, considerando una masa de 100 g de muestra de compost. Así, tenemos: 40 g de C, 6,67 g de H y 53,33 g de O.
Ahora es necesario pasar estos valores a la cantidad de materia (mol). Hacemos esto dividiendo cada uno de los valores encontrados por sus respectivas masas molares:
C: 40/12 = 3,33
H: 6,67 / 1 = 6,67
O: 53,33 / 16 = 3,33
Dado que los valores no son números enteros, utilizamos el siguiente dispositivo: dividimos todos los valores por el más pequeño de ellos, para que la proporción entre ellos no cambie.
En este caso, el valor más pequeño es 3.33, por lo que el resultado será:
C: 3,33 / 3,33 = 1
H: 6,67 / 3,33 = 2
O: 3.33 / 3.33 = 1
Así, la fórmula mínima de esta sustancia desconocida es igual a: C1H2O1 o CH2O.
Brevemente, los pasos necesarios para encontrar la fórmula empírica o mínima de una sustancia son:

Por Jennifer Fogaça
Licenciada en Química
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
FOGAÇA, Jennifer Rocha Vargas. "Fórmula mínima o empírica"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/formula-minima-ou-empirica.htm. Consultado el 28 de junio de 2021.


